Tin tức
Mạng tinh thể là gì? cấu trúc, đặc điểm và ứng dụng
Mạng tinh thể là khái niệm nền tảng quyết định đặc tính của vô số vật liệu trong tự nhiên và công nghiệp. Từ hạt muối ăn (NaCl) trong bếp, độ cứng vượt trội của kim cương, cho đến tấm silicon tinh khiết trong mọi con chip máy tính, tất cả đều được quyết định bởi cấu trúc vi mô này.
Hiểu về mạng tinh thể là chìa khóa để làm chủ khoa học vật liệu, dự đoán tính chất và tạo ra các ứng dụng đột phá. Bài viết này cung cấp một hướng dẫn chi tiết, toàn diện về mạng tinh thể, bao gồm định nghĩa, phân loại, các đặc điểm và ứng dụng thực tiễn quan trọng nhất.
Mạng Tinh Thể Là Gì?
Mạng tinh thể là một cấu trúc không gian 3D, nơi các nguyên tử, ion, hoặc phân tử được sắp xếp theo một trật tự lặp lại tuần hoàn, đều đặn. Cấu trúc trật tự này quyết định các tính chất vật lý và hóa học đặc trưng của vật rắn.
Mạng tinh thể (hay mạng tinh thể Bravais) là cấu trúc không gian ba chiều (3D), trong đó các hạt cấu tạo nên vật rắn—bao gồm nguyên tử, ion, hoặc phân tử—được sắp xếp theo một trật tự lặp lại tuần hoàn và đều đặn trong không gian.
Hãy tưởng tượng nó như một “bộ khung” vô hình, cực kỳ trật tự, quyết định mọi thứ, từ hình dạng bên ngoài đến các tính chất vật lý và hóa học của vật liệu, như độ cứng, khả năng dẫn điện, và nhiệt độ nóng chảy.
Các Thành Phần Cốt Lõi Của Mạng Tinh Thể
Ba thành phần cốt lõi của mạng tinh thể bao gồm: Nút mạng (vị trí cố định của hạt), Ô cơ sở (đơn vị cấu trúc nhỏ nhất lặp đi lặp lại), và Liên kết hóa học (lực giữ các hạt lại với nhau, ví dụ: liên kết ion, cộng hóa trị, kim loại).
Để hiểu rõ một mạng tinh thể, chúng ta cần nắm được ba thành phần cơ bản của nó:
- Nút mạng (Lattice Point): Đây là các vị trí cố định trong không gian nơi các hạt (nguyên tử, ion, phân tử) cư ngụ.
- Ô cơ sở (Unit Cell): Là đơn vị cấu trúc nhỏ nhất, mang tính đại diện cho toàn bộ mạng tinh thể. Khi bạn lặp lại ô cơ sở này theo cả ba chiều không gian, bạn sẽ thu được toàn bộ tinh thể. Ô cơ sở quyết định hình dạng và kích thước của mạng.
- Liên kết hóa học: “Chất keo” giữ các hạt lại với nhau tại các nút mạng. Loại liên kết này quyết định mạnh mẽ tính chất của tinh thể:
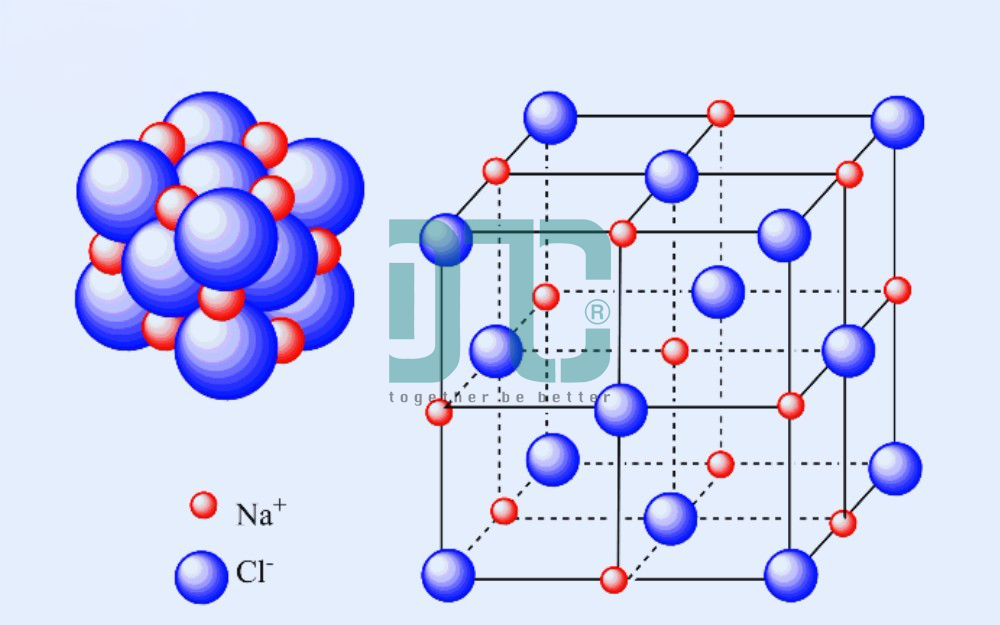
- Liên kết Ion: Thấy trong các muối, như muối ăn (NaCl). Các cation (như Na⁺) và anion (như Cl⁻) hút nhau bằng lực tĩnh điện. Xem thêm về hợp chất này tại bài viết NaCl + H₂O.
- Liên kết cộng hóa trị: Các nguyên tử dùng chung electron, tạo ra liên kết cực kỳ bền chắc. Ví dụ kinh điển là kim cương.
- Liên kết kim loại: Các ion dương kim loại nằm trong một “biển” electron tự do, giúp kim loại dẫn điện tốt.
Phân Loại Các Mạng Tinh Thể Phổ Biến
Có 14 mạng Bravais (mạng tinh thể) cơ bản, được phân loại dựa trên hình học của ô cơ sở. Các loại phổ biến nhất bao gồm: Lập phương tâm khối (BCC) (ví dụ: Sắt, Crom), Lập phương tâm diện (FCC) (ví dụ: Vàng, Đồng), và Lục giác xếp chặt (HCP) (ví dụ: Kẽm, Magie).
Dựa trên hình học của ô cơ sở và cách sắp xếp các nút mạng, có 14 loại mạng Bravais, nhưng chúng ta thường tập trung vào các nhóm chính sau:
a. Mạng Lập Phương (Cubic)
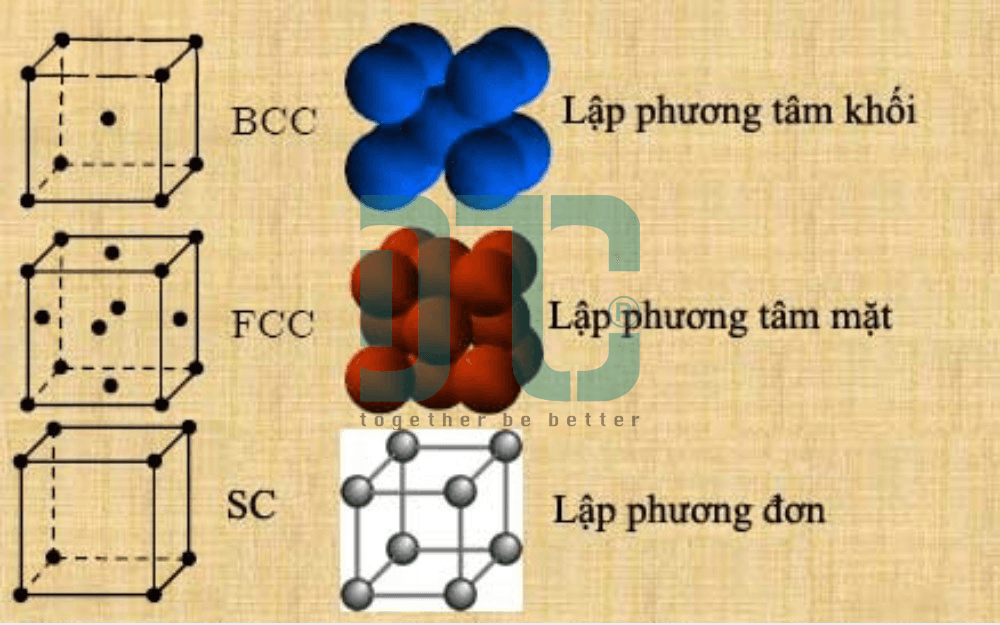
Mạng lập phương có ô cơ sở là hình lập phương, là dạng phổ biến nhất. Ba kiểu chính là: Đơn giản (SC) (nút ở 8 góc), Tâm khối (BCC) (thêm 1 nút ở tâm khối), và Tâm diện (FCC) (thêm 6 nút ở tâm 6 mặt).
Đây là dạng phổ biến và đơn giản nhất, với ô cơ sở là hình lập phương.
- Lập phương đơn giản (Simple Cubic – SC): Các hạt chỉ nằm ở 8 góc của khối lập phương. (Ví dụ: Polonium).
- Lập phương tâm khối (Body-Centered Cubic – BCC): Ngoài 8 hạt ở góc, có thêm 1 hạt nằm ngay tại tâm khối. (Ví dụ: Sắt alpha, Crom, Natri (Na)).
- Lập phương tâm diện (Face-Centered Cubic – FCC): Ngoài 8 hạt ở góc, có thêm 6 hạt nằm ở tâm của 6 mặt. Đây là cấu trúc xếp đặc khít. (Ví dụ: Vàng, Đồng, Nhôm, Chì (Pb)).
b. Mạng Lục Giác (Hexagonal)
Mạng lục giác có ô cơ sở hình lăng trụ lục giác. Dạng Lục giác xếp chặt (HCP) là cấu trúc có mật độ đóng gói nguyên tử cao, tương tự FCC, và phổ biến ở nhiều kim loại như Kẽm (Zn), Magie (Mg) và Titan.
Cấu trúc này gồm các lớp hạt xếp chồng lên nhau một cách hiệu quả, phổ biến với nhiều kim loại.
- Lục giác xếp chặt (Hexagonal Close-Packed – HCP): (Ví dụ: Titan, Magie (Mg), Kẽm (Zn)).
c. Các Cấu Trúc Khác
Ngoài Lập phương và Lục giác, còn có các hệ tinh thể khác như Tứ giác (Tetragonal), Trực thoi (Orthorhombic), Tam nghiêng (Triclinic)… Chúng phổ biến trong các khoáng chất, vật liệu gốm sứ, và các hợp chất hữu cơ hay polymer phức tạp.
Ngoài ra còn có các cấu trúc phức tạp hơn như Tứ giác (Tetragonal), Tam nghiêng (Triclinic), Ba nghiêng (Monoclinic)… thường thấy trong các khoáng chất, polymer hoặc vật liệu hữu cơ phức tạp.
Để xác định chính xác loại mạng tinh thể của một vật liệu, các nhà khoa học sử dụng các kỹ thuật phân tích hiện đại, phổ biến nhất là Nhiễu xạ Tia X (XRD).
Đặc Điểm Nổi Bật Quyết Định Tính Chất Vật Liệu
Cấu trúc mạng tinh thể quyết định trực tiếp các tính chất vĩ mô. Ví dụ: Mạng lưới liên kết cộng hóa trị chặt chẽ của kim cương tạo ra độ cứng vô địch; mạng lưới có electron tự do của kim loại (cấu trúc FCC, BCC) tạo ra tính dẫn điện; cấu trúc đối xứng của thạch anh tạo ra các tính chất quang học đặc biệt.
Cấu trúc mạng tinh thể ảnh hưởng trực tiếp đến các đặc tính vật lý mà chúng ta có thể quan sát và đo lường.
Độ cứng và Độ bền
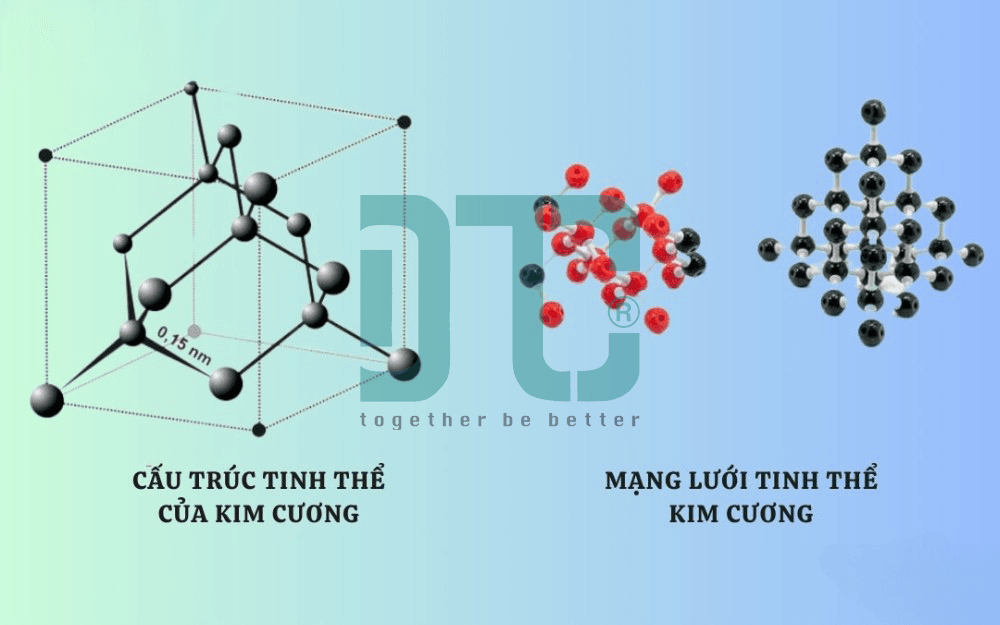
- Kim cương: Là vật liệu cứng nhất tự nhiên (10 trên thang Mohs). Lý do là mạng tinh thể của nó tạo thành từ các nguyên tử Cacbon (C) liên kết cộng hóa trị tứ diện cực kỳ chặt chẽ.
- Graphite (Than chì): Trớ trêu thay, graphite cũng được tạo nên hoàn toàn từ Cacbon. Nhưng do cấu trúc mạng tinh thể dạng lớp, các lớp liên kết yếu với nhau nên graphite lại rất mềm và được dùng làm ruột bút chì.
Tính Dẫn Điện và Dẫn Nhiệt
- Chất dẫn điện: Các kim loại dẫn điện tốt (như Đồng, Vàng) thường có cấu trúc FCC hoặc BCC, cho phép các electron tự do di chuyển dễ dàng qua mạng lưới.
- Chất cách điện: Trong kim cương hoặc muối ăn (NaCl), các electron bị “khóa” chặt trong các liên kết ion hoặc cộng hóa trị, không thể di chuyển tự do, khiến chúng cách điện hoàn toàn.
- Chất bán dẫn: Silicon (Si) có cấu trúc mạng giống kim cương. Ở trạng thái tinh khiết, nó cách điện. Nhưng khi thêm một lượng nhỏ tạp chất (gọi là “doping”), ví dụ như Boron (B) hoặc Phospho (P), tính dẫn điện của nó thay đổi đáng kể, tạo nên nền tảng của ngành công nghiệp điện tử.
Tính Chất Quang Học
- Tính đối xứng cao của mạng tinh thể quyết định cách vật liệu tương tác với ánh sáng.
- Thạch anh (Silic Dioxit – SiO₂) có khả năng làm quay mặt phẳng ánh sáng phân cực, được dùng trong các thiết bị quang học chính xác.
- Đá quý như Ruby và Sapphire thực chất là tinh thể Oxit nhôm (Al₂O₃). Cấu trúc tinh thể hoàn hảo của chúng cho phép ánh sáng truyền qua, tán sắc và phản xạ, tạo nên vẻ đẹp lấp lánh.
Ứng Dụng Thực Tiễn Của Mạng Tinh Thể
Ứng dụng của mạng tinh thể có mặt trong mọi lĩnh vực: Công nghiệp điện tử (tinh thể Silicon làm chip, pin mặt trời), Ngành trang sức (Kim cương, Ruby), Vật liệu xây dựng (mạng tinh thể khoáng chất trong bê tông, gốm sứ), Dược phẩm (các dạng tinh thể thuốc ảnh hưởng đến độ tan), và Quang học (tinh thể thạch anh làm cáp quang).
Mạng tinh thể là cốt lõi của khoa học vật liệu và có mặt trong mọi khía cạnh của đời sống:
- Công Nghiệp Điện Tử: Silicon tinh thể đơn (monocrystalline silicon) là “trái tim” của chip máy tính, bóng bán dẫn, tấm pin mặt trời và các loại cảm biến nhiệt độ. Toàn bộ ngành công nghệ bán dẫn dựa trên việc kiểm soát cấu trúc tinh thể của silicon.
- Ngành Trang Sức: Kim cương, Ruby, Sapphire… có giá trị cao nhờ độ cứng và vẻ đẹp quang học, tất cả đều đến từ cấu trúc mạng tinh thể hoàn hảo của chúng.
- Vật Liệu Xây Dựng: Xi măng, bê tông và gốm sứ đạt được độ bền cơ học nhờ vào cấu trúc mạng tinh thể của các khoáng chất như canxi silicat hay đá vôi (CaCO₃).
- Hóa Học và Dược Phẩm: Trong ngành dược, các dạng tinh thể khác nhau của cùng một hoạt chất (gọi là đa hình – polymorphs) có thể ảnh hưởng lớn đến độ tan, độ ổn định và khả năng hấp thụ của thuốc trong cơ thể.
- Công Nghiệp Quang Học và Viễn Thông: Tinh thể thạch anh (SiO₂) được sử dụng để chế tạo các bộ cộng hưởng tần số chính xác trong đồng hồ, máy tính và là vật liệu cốt lõi của cáp quang.
Kết Luận
Mạng tinh thể không chỉ là một khái niệm trừu tượng trong sách giáo khoa hóa học hay vật lý. Đó là “kiến trúc sư” thầm lặng định hình thế giới vật chất xung quanh chúng ta. Từ kim loại ta dùng hàng ngày, con chip trong điện thoại, đến viên đá quý lấp lánh, tất cả đều tuân theo các quy luật sắp xếp trật tự của mạng tinh thể.
Bằng cách hiểu và kiểm soát các cấu trúc này, con người tiếp tục tạo ra những vật liệu mới với các đặc tính ưu việt, thúc đẩy công nghệ và cải thiện cuộc sống.
Nguồn tham khảo:
- Callister, W. D., & Rethwisch, D. G. (2020). Materials Science and Engineering: An Introduction.
- Kittel, C. (2004). Introduction to Solid State Physics.
- Web: https://www.materialsproject.org, https://www.ccdc.cam.ac.uk
Người kiểm duyệt nội dung
PGS.TS Đặng Hoàng Phú
Cố vấn chuyên môn cấp cao tại Hóa Chất Doanh Tín. Phó Giáo sư, Giảng viên Khoa Hóa học (ĐH KHTN ĐHQG-HCM) với hơn 10 năm kinh nghiệm nghiên cứu Hóa hữu cơ & Phổ nghiệm.
Xem hồ sơ năng lực & công bố khoa học →









