Kiến thức chuyên môn
Hidrocacbon No (Ankan) Là Gì? Lý Thuyết & Bài Tập Hóa 11 (2025)
💡
Bạn đã bao giờ tự hỏi thành phần chính của khí gas, xăng xe hay khí tự nhiên là gì chưa? Câu trả lời nằm ở hidrocacbon no, một trong những khái niệm nền tảng và quan trọng nhất của hóa học hữu cơ.
Bài viết chuyên sâu này từ Hóa Chất Doanh Tín sẽ cung cấp cho bạn cái nhìn chi tiết nhất: từ định nghĩa khoa học, công thức tổng quát, tính chất đặc trưng cho đến những ứng dụng thực tiễn không thể thiếu trong đời sống và công nghiệp hiện đại.
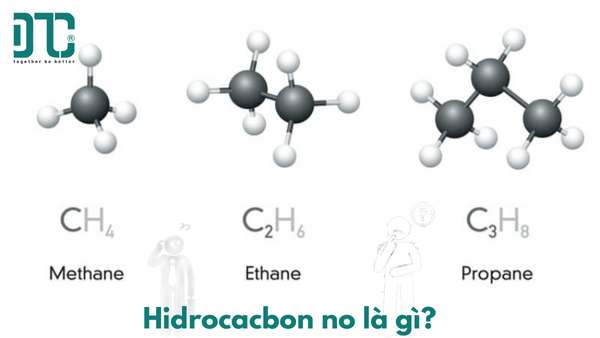
Hidrocacbon No Là Gì? Định Nghĩa & Công Thức Tổng Quát
Định nghĩa cốt lõi: Hidrocacbon no (hay Ankan) là những hợp chất hữu cơ mà trong phân tử chỉ chứa liên kết đơn (liên kết
) bền vững giữa các nguyên tử Cacbon (C) và Hidro (H).
Chúng được gọi là “no” (bão hòa) vì các nguyên tử cacbon đã sử dụng hết khả năng liên kết của mình với hidro, do đó không thể tham gia phản ứng cộng để nhận thêm bất kỳ nguyên tử nào khác. Công thức tổng quát cho dãy đồng đẳng của ankan là:
Ví dụ kinh điển về hidrocacbon no:
- Metan (CH₄):
 . Là thành phần chính của khí thiên nhiên (75-97%) và khí biogas.
. Là thành phần chính của khí thiên nhiên (75-97%) và khí biogas. - Etan (C₂H₆):
 . Có nhiều trong khí đồng hành của các mỏ dầu.
. Có nhiều trong khí đồng hành của các mỏ dầu. - Propan (C₃H₈) & Butan (C₄H₁₀): Hỗn hợp của hai khí này chính là khí gas hóa lỏng (LPG) dùng để đun nấu hàng ngày.

Mô hình phân tử của 4 ankan đầu dãy đồng đẳng.
Đặc Điểm Cấu Tạo & Tính Chất Vật Lý
Cấu trúc phân tử bền vững
Trong phân tử hidrocacbon no, các nguyên tử cacbon ở trạng thái lai hóa ![]() . Điều này tạo nên cấu trúc không gian tứ diện đều (với góc liên kết khoảng
. Điều này tạo nên cấu trúc không gian tứ diện đều (với góc liên kết khoảng ![]() ). Liên kết
). Liên kết ![]() (sigma) rất bền vững, khó bị phá vỡ ở điều kiện thường. Đây là lý do tại sao ankan còn có tên gọi là Parafin (tiếng Latinh *parum affinis* nghĩa là “ít ái lực hóa học”).
(sigma) rất bền vững, khó bị phá vỡ ở điều kiện thường. Đây là lý do tại sao ankan còn có tên gọi là Parafin (tiếng Latinh *parum affinis* nghĩa là “ít ái lực hóa học”).
Quy luật biến đổi tính chất vật lý
| Số nguyên tử Cacbon | Trạng thái (đk thường) | Ví dụ thực tế |
|---|---|---|
| Chất Khí | Gas, khí bioga | |
| Chất Lỏng | Xăng, dầu hỏa, dung môi | |
| Chất Rắn | Nến, nhựa đường, sáp |
Quy luật chung: Khi số nguyên tử Cacbon tăng ![]() Phân tử khối tăng
Phân tử khối tăng ![]() Lực tương tác Van der Waals tăng
Lực tương tác Van der Waals tăng ![]() Nhiệt độ sôi và nhiệt độ nóng chảy tăng dần.
Nhiệt độ sôi và nhiệt độ nóng chảy tăng dần.
Tính tan: Hidrocacbon no là những dung môi không phân cực. Do đó, chúng không tan trong nước (nhẹ hơn nước nên nổi lên trên) nhưng tan tốt trong các dung môi hữu cơ khác như dầu mỡ. Đây là nguyên lý để dùng xăng dầu tẩy vết bẩn dầu mỡ.
Tính Chất Hóa Học Đặc Trưng
Mặc dù khá trơ ở điều kiện thường, nhưng dưới tác dụng của nhiệt độ, xúc tác và ánh sáng, hidrocacbon no tham gia 3 loại phản ứng quan trọng sau:
a. Phản ứng Thế Halogen (Đặc trưng nhất)
Khi có ánh sáng khuếch tán (askt) hoặc nhiệt độ, nguyên tử Hidro trong ankan sẽ bị thay thế bởi nguyên tử Halogen (Clo, Brom).
Quy tắc thế: Nguyên tử Halogen sẽ ưu tiên thế vào nguyên tử Cacbon bậc cao hơn (Cacbon liên kết với ít Hidro hơn).
b. Phản ứng Tách (Cracking & Tách Hidro)
Dưới tác dụng của nhiệt độ cao và xúc tác, mạch cacbon dài bị bẻ gãy thành mạch ngắn hơn (Cracking) hoặc tách bớt hidro để tạo thành liên kết đôi (Anken).
- Cracking:

- Tách Hidro:

Đây là phản ứng sống còn của công nghiệp lọc hóa dầu để sản xuất xăng và nguyên liệu nhựa.
c. Phản ứng Oxi hóa (Phản ứng Cháy)
Phản ứng này tỏa ra nhiệt lượng cực lớn, là cơ sở để sử dụng ankan làm nhiên liệu.
Ứng Dụng Thực Tế & Cách Nhận Biết
🔥 Nhiên liệu năng lượng
Khí đốt (Gas), xăng xe máy, dầu diesel cho ô tô, nhiên liệu phản lực cho máy bay. Đây là nguồn năng lượng chính vận hành nền kinh tế toàn cầu.
🏭 Nguyên liệu hóa dầu
Dùng để sản xuất nhựa (PE, PP), cao su tổng hợp, dung môi pha sơn, và hàng ngàn hợp chất hữu cơ khác.
💊 Y tế & Mỹ phẩm
Vaseline (sáp nẻ), nến parafin, dầu khoáng (mineral oil) trong mỹ phẩm dưỡng da.
Cách nhận biết Hidrocacbon no
Để phân biệt Ankan với các hidrocacbon khác, ta dựa vào tính “trơ” của nó:
- Dung dịch Brom/Thuốc tím (
 ): Ankan KHÔNG làm mất màu các dung dịch này ở điều kiện thường (Khác biệt hoàn toàn với Anken/Ankin).
): Ankan KHÔNG làm mất màu các dung dịch này ở điều kiện thường (Khác biệt hoàn toàn với Anken/Ankin). - Quỳ tím: Không đổi màu (do không có tính axit/bazo).
Câu Hỏi Thường Gặp (FAQ)
1. Tại sao ankan lại tương đối trơ về mặt hóa học?
Do phân tử chỉ chứa các liên kết ![]() (C-C, C-H) rất bền vững, cần năng lượng kích hoạt lớn mới có thể phá vỡ. Vì vậy chúng không phản ứng với axit, bazơ hay chất oxi hóa mạnh ở nhiệt độ thường.
(C-C, C-H) rất bền vững, cần năng lượng kích hoạt lớn mới có thể phá vỡ. Vì vậy chúng không phản ứng với axit, bazơ hay chất oxi hóa mạnh ở nhiệt độ thường.
2. Cracking ankan có ý nghĩa gì?
Cracking giúp biến các ankan mạch dài (ít giá trị, khó cháy) thành các ankan mạch ngắn (xăng) và anken (nguyên liệu sản xuất nhựa). Đây là “trái tim” của nhà máy lọc dầu.
3. Khí metan có độc không?
Metan không độc trực tiếp nhưng gây ngạt thở nếu nồng độ quá cao (chiếm chỗ oxy). Đặc biệt, hỗn hợp Metan và Oxy là hỗn hợp nổ mạnh, rất nguy hiểm trong các hầm lò khai thác than.
Hy vọng bài viết chuyên sâu này từ Hóa Chất Doanh Tín đã giúp bạn nắm vững kiến thức về Hidrocacbon no. Nếu bạn có nhu cầu về dung môi công nghiệp hay hóa chất thí nghiệm, đừng ngần ngại liên hệ với chúng tôi để được tư vấn kỹ thuật miễn phí!
Người kiểm duyệt nội dung
PGS.TS Đặng Hoàng Phú
Cố vấn chuyên môn cấp cao tại Hóa Chất Doanh Tín. Phó Giáo sư, Giảng viên Khoa Hóa học (ĐH KHTN ĐHQG-HCM) với hơn 10 năm kinh nghiệm nghiên cứu Hóa hữu cơ & Phổ nghiệm.
Xem hồ sơ năng lực & công bố khoa học →









