Kiến thức chuyên môn
Ethanol Là Gì? Phân Loại, Ứng Dụng & Tiêu Chuẩn An Toàn
Ethanol, thường được biết đến với tên gọi cồn công nghiệp, không chỉ là thành phần chính trong xăng sinh học mà còn là một dung môi và hợp chất nền tảng không thể thiếu trong vô số ngành công nghiệp. Để khai thác tối đa tiềm năng và đảm bảo an toàn, việc hiểu rõ bản chất, cấp độ tinh khiết và tiêu chuẩn kỹ thuật của Ethanol là yêu cầu bắt buộc.
Với kinh nghiệm chuyên sâu, Hóa Chất Doanh Tín sẽ cung cấp một góc nhìn toàn diện, từ cấu trúc phân tử của hợp chất hữu cơ này đến các ứng dụng thực tiễn và những lưu ý an toàn quan trọng theo quy định tại Việt Nam.
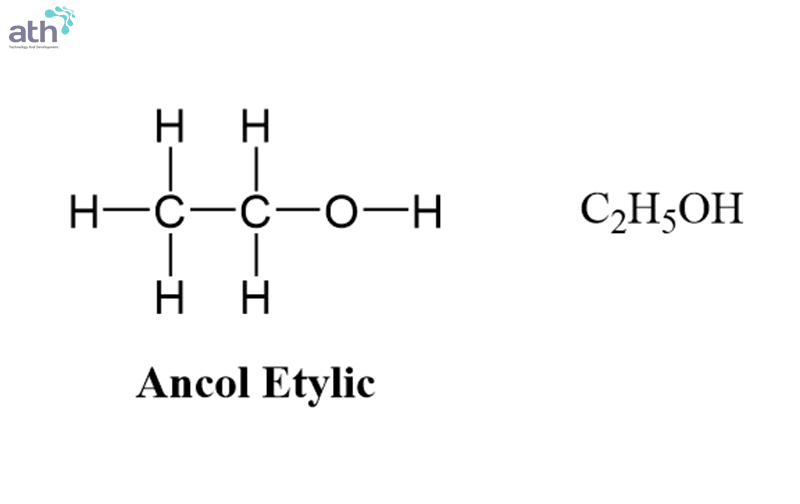
1. Ethanol là gì, có định nghĩa kỹ thuật và tên gọi nào?
Ethanol (C₂H₅OH) là một hợp chất hữu cơ thuộc dãy đồng đẳng của ancol, còn được biết đến với các tên gọi như Rượu Etylic, Cồn Công Nghiệp, Etanol, Ethanol Tuyệt Đối, và Ethanol Biến Tính.

Ethanol, với công thức hóa học là C₂H₅OH, là một ancol đơn chức, mạch hở. Trong hệ thống danh pháp hóa học quốc tế (IUPAC), nó được gọi là Etanol. Sự đa dạng trong tên gọi của nó phản ánh vai trò và ứng dụng rộng rãi trong nhiều lĩnh vực khác nhau. “Rượu Etylic” là tên gọi phổ thông nhất, trong khi “Cồn Công Nghiệp” thường chỉ loại ethanol 96% trở lên không dùng cho thực phẩm. “Ethanol Tuyệt Đối” có độ tinh khiết trên 99.5%, và “Ethanol Biến Tính” đã được thêm phụ gia để không thể uống, nhằm mục đích công nghiệp và tránh thuế tiêu thụ đặc biệt.
2. Ethanol có những tính chất lý hóa đặc trưng nào?
2.1. Các tính chất vật lý nổi bật của Ethanol là gì?
Ethanol là một chất lỏng không màu, trong suốt, có mùi thơm nhẹ, dễ bay hơi, tan vô hạn trong nước, có nhiệt độ sôi 78.37°C và nhiệt độ đông đặc -114.1°C.
Về mặt vật lý, Ethanol có khối lượng riêng khoảng 0.789 g/cm³, nhẹ hơn nước. Đặc tính tan vô hạn trong nước của nó là do khả năng hình thành liên kết hydro mạnh mẽ giữa nhóm hydroxyl (-OH) của Ethanol và các phân tử nước. Nhiệt độ đông đặc rất thấp của nó cũng là một đặc tính quan trọng, giúp nó trở thành một thành phần hiệu quả trong các dung dịch chống đông.
2.2. Các tính chất hóa học cốt lõi của Ethanol là gì?
Ethanol thể hiện đầy đủ các tính chất hóa học của một ancol đơn chức, bao gồm phản ứng với kim loại kiềm, phản ứng este hóa, phản ứng tách nước và phản ứng oxy hóa (hoàn toàn và không hoàn toàn).
Ethanol có khả năng tham gia vào nhiều phản ứng hóa học quan trọng. Nó phản ứng với các kim loại kiềm như Natri (Na) để giải phóng khí hydro. Một trong những phản ứng đặc trưng nhất là phản ứng este hóa với axit hữu cơ để tạo ra este, ví dụ như tạo ra etyl axetat. Phản ứng tách nước của Ethanol có thể tạo ra etylen (anken) ở 170°C. Ngoài ra, nó có thể bị oxy hóa không hoàn toàn để tạo ra anđehit axetic, hoặc cháy hoàn toàn trong một phản ứng tỏa nhiệt mạnh, tạo ra CO₂ và nước.
Ethanol mang những tính chất đặc trưng của một rượu đơn chức, cụ thể như sau:
- Tác dụng với kim loại:
2C2H5OH + 2Na → 2C2H5ONa + H2
- Tác dụng với Cu(OH)2
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O
- Phản ứng với axit vô cơ:
C2H5-OH + H-Br → C2H5-Br + H2O
- Tác dụng với axit hữu cơ (phản ứng este hóa):
CH3COOH + C2H5-OH → CH3COOC2H5 + H2O
- Tham gia phản ứng với ancol (Trong điều kiện phản ứng H2SO4 đậm đặc, 1400C):
C2H5-OH + H-O-C2H5 → C2H5-O-C2H5 + H2O
- Tham gia phản ứng tách nhóm -OH (phản ứng tách H2O) (Trong điều kiện phản ứng H2SO4 đậm đặc, 1700C):
CH3-CH2-OH → CH2=CH2 + H2O
CH3-CH2-CHOH-CH3 → H2O + CH3-CH=CH-CH3 (sản phẩm chính)
→ H2O + CH3-CH2-CH=CH2 (sản phẩm phụ)
- Tham gia phản ứng oxi hóa không hoàn toàn (oxi hóa hữu hạn):
C2H5OH + CuO → CH3-CHO + H2O + Cu
3. Quy trình sản xuất và điều chế Ethanol trong công nghiệp như thế nào?
3.1. Phương pháp sản xuất sinh học (lên men) là gì?
Đây là phương pháp sản xuất Ethanol bằng cách lên men các nguyên liệu tự nhiên chứa carbohydrate như ngô, sắn, mía, thông qua quá trình chuyển hóa tinh bột thành đường glucose và sau đó thành Ethanol nhờ nấm men.

Phương pháp sinh học là quy trình truyền thống và bền vững để sản xuất Ethanol. Nó bắt đầu bằng việc thủy phân tinh bột từ các nguồn nông sản thành đường glucose. Sau đó, trong điều kiện yếm khí, các chủng nấm men (chủ yếu là Saccharomyces cerevisiae) sẽ lên men glucose để tạo ra Ethanol và carbon dioxide. Ethanol sản xuất bằng phương pháp này thường có chất lượng cao và được ưu tiên sử dụng trong ngành thực phẩm và dược phẩm.
3.2. Phương pháp tổng hợp hóa dầu (hydrat hóa etylen) là gì?
Đây là phương pháp công nghiệp hiện đại sản xuất Ethanol bằng cách cho etylen (C₂H₄) phản ứng với nước dưới điều kiện nhiệt độ, áp suất cao và có chất xúc tác axit.
Sản xuất Ethanol từ etylen là một quy trình hóa dầu quy mô lớn. Phản ứng hydrat hóa trực tiếp etylen (một sản phẩm từ quá trình cracking dầu mỏ) với hơi nước thường sử dụng axit photphoric làm chất xúc tác. Phương pháp này tạo ra Ethanol có độ tinh khiết cao với chi phí sản xuất thấp, là nguồn cung chính cho các ứng dụng công nghiệp như dung môi và nguyên liệu sản xuất hóa chất khác.
“Từ góc độ của một nhà cung cấp, chúng tôi nhận thấy việc lựa chọn nguồn gốc Ethanol là cực kỳ quan trọng. Ethanol từ lên men sinh học, với độ tinh khiết cao và không lẫn tạp chất từ hóa dầu, là lựa chọn bắt buộc cho ngành thực phẩm và dược phẩm. Trong khi đó, Ethanol tổng hợp lại có ưu thế về giá thành và sản lượng lớn, đáp ứng hoàn hảo cho các ứng dụng dung môi công nghiệp quy mô lớn. Việc hiểu rõ quy trình sản xuất giúp khách hàng của chúng tôi đưa ra quyết định mua hàng thông minh và hiệu quả nhất.” – Nguyễn Thị Mỹ Linh, Chuyên gia Kỹ thuật Hóa chất, Doanh Tín.
4. Vai trò chiến lược của Ethanol trong các ngành công nghiệp là gì?
4.1. Vai trò của Ethanol trong ngành năng lượng là gì?
Ethanol là thành phần chính trong nhiên liệu sinh học, được pha vào xăng để tạo ra xăng sinh học E10 và E5, giúp tăng chỉ số octan và giảm phát thải khí nhà kính.
Trong ngành năng lượng, Ethanol đóng vai trò là một nhiên liệu tái tạo quan trọng. Việc pha trộn Ethanol vào xăng không chỉ giúp giảm sự phụ thuộc vào nhiên liệu hóa thạch mà còn cải thiện hiệu suất đốt cháy của động cơ. Theo các nghiên cứu gần đây, việc sử dụng xăng E10 có thể giúp giảm tới 2-3% lượng khí thải CO₂ so với xăng thông thường.
4.2. Vai trò của Ethanol trong ngành hóa chất và sản xuất là gì?
Ethanol là một dung môi công nghiệp đa năng, một nguyên liệu tổng hợp quan trọng để sản xuất các hóa chất khác, và là một chất chống đông hiệu quả.
Với khả năng hòa tan tốt nhiều chất, Ethanol được sử dụng rộng rãi làm dung môi trong sản xuất sơn, mực in, dược phẩm và mỹ phẩm. Nó cũng là tiền chất để sản xuất nhiều hợp chất hữu cơ quan trọng như axit axetic và etyl axetat. Đặc tính chống đông của nó được ứng dụng trong các dung dịch làm mát động cơ và chất tẩy rửa kính ô tô.
4.3. Vai trò của Ethanol trong ngành y tế và dược phẩm là gì?
Ethanol, dưới dạng cồn y tế 70%, là một chất sát khuẩn bề mặt hiệu quả. Nó cũng được dùng làm dung môi trong sản xuất thuốc và chiết xuất dược liệu.
Trong y tế, dung dịch Ethanol 70% được coi là “tiêu chuẩn vàng” để sát khuẩn do khả năng thẩm thấu qua màng tế bào vi sinh vật và làm đông tụ protein của chúng. Ngoài ra, nó còn được sử dụng làm dung môi để hòa tan các hoạt chất trong sản xuất siro, thuốc bôi, và để sản xuất các chất khử trùng mạnh hơn như Chloramin B.
… (Giữ nguyên mục 4.4 và 4.5) …
5. Sự khác biệt giữa Ethanol, Methanol và Isopropanol là gì?
Điểm khác biệt cốt lõi nằm ở độc tính và ứng dụng: Ethanol có độc tính thấp và có thể dùng trong thực phẩm (loại tinh khiết), trong khi Methanol (CH₃OH) cực độc, và Isopropanol (IPA) chỉ dùng ngoài da, không được uống.
Việc phân biệt các loại cồn này là vấn đề an toàn sống còn. Methanol, hay cồn công nghiệp gỗ, có thể gây mù lòa hoặc tử vong nếu uống phải dù chỉ một lượng nhỏ. Isopropanol, hay cồn tẩy rửa, có độc tính cao hơn Ethanol và chỉ được sử dụng cho mục đích sát khuẩn ngoài da hoặc làm dung môi công nghiệp. Luôn kiểm tra nhãn mác và nguồn gốc sản phẩm để đảm bảo sử dụng đúng loại cồn cho đúng mục đích.
… (Giữ nguyên Bảng so sánh) …
6. Các tiêu chuẩn an toàn khi sử dụng và bảo quản Ethanol là gì?
6.1. Nguyên tắc bảo quản Ethanol an toàn là gì?
Ethanol phải được lưu trữ trong khu vực khô ráo, thoáng mát, tránh xa nguồn nhiệt và tia lửa, trong các thùng chứa chuyên dụng có dán nhãn cảnh báo nguy hiểm rõ ràng.
Việc bảo quản hóa chất dễ cháy như Ethanol đòi hỏi sự tuân thủ nghiêm ngặt. Khu vực kho chứa phải có hệ thống thông gió tốt và được trang bị đầy đủ các thiết bị phòng cháy chữa cháy phù hợp cho đám cháy chất lỏng (ví dụ: bình chữa cháy CO₂ hoặc bột). Nhãn trên thùng chứa phải tuân thủ tiêu chuẩn GHS, cung cấp thông tin rõ ràng về các mối nguy.
6.2. Cần có những lưu ý gì khi sử dụng Ethanol?
Khi sử dụng Ethanol, đặc biệt ở nồng độ cao, cần phải đeo đầy đủ trang bị bảo hộ cá nhân (PPE) như kính mắt, găng tay, và đảm bảo khu vực làm việc được thông gió tốt.
Để tránh các rủi ro về sức khỏe do hít phải hơi Ethanol nồng độ cao hoặc tiếp xúc qua da, việc sử dụng PPE là bắt buộc. Kính bảo hộ giúp ngăn hóa chất bắn vào mắt, và găng tay chống hóa chất bảo vệ da tay. Hệ thống thông gió đầy đủ giúp ngăn ngừa sự tích tụ của hơi Ethanol trong không khí, giảm nguy cơ cháy nổ và các vấn đề về hô hấp.
6.3. Cần tuân thủ những quy định nào của Việt Nam?
Việc sản xuất, kinh doanh và sử dụng Ethanol tại Việt Nam phải tuân thủ các Tiêu chuẩn Việt Nam (TCVN) liên quan và các quy định trong Luật Hóa Chất mới nhất.
Các doanh nghiệp hoạt động trong lĩnh vực này phải nắm rõ và tuân thủ các TCVN về yêu cầu kỹ thuật, phương pháp thử, và an toàn hóa chất. Luật Hóa Chất của Việt Nam quy định chi tiết về việc khai báo, phân loại, ghi nhãn, và vận chuyển hóa chất nguy hiểm, bao gồm cả Ethanol, để đảm bảo an toàn cho con người và môi trường.
Người kiểm duyệt nội dung
PGS.TS Đặng Hoàng Phú
Cố vấn chuyên môn cấp cao tại Hóa Chất Doanh Tín. Phó Giáo sư, Giảng viên Khoa Hóa học (ĐH KHTN ĐHQG-HCM) với hơn 10 năm kinh nghiệm nghiên cứu Hóa hữu cơ & Phổ nghiệm.
Xem hồ sơ năng lực & công bố khoa học →









