Kiến thức chuyên môn
Chloroform (CHCl₃) là gì? Đặc điểm, ứng dụng, độc tính và cách sử dụng an toàn
Chloroform (CHCl₃) là hợp chất hữu cơ thuộc nhóm trihalomethane, chất lỏng không màu, dễ bay hơi, có mùi ngọt đặc trưng, dùng làm dung môi hòa tan chất béo, cao su, alkaloid và làm tiền chất sản xuất chất làm lạnh, PTFE. Nó có độc tính cao, gây hại gan, thận, hệ thần kinh khi hít hoặc nuốt, và được phân loại là chất nghi gây ung thư (IARC Group 2B).
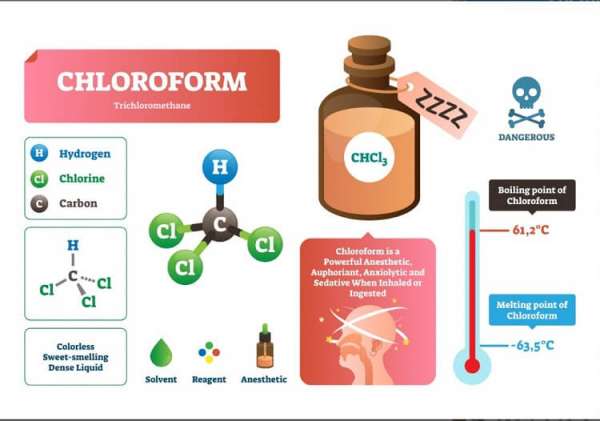
Tính Chất Vật Lý Của Chloroform
Chloroform là chất lỏng trong suốt, không màu, mùi ngọt giống ether, mật độ 1.489 g/cm³ ở 25°C, điểm sôi 61.15°C, dễ bay hơi ở nhiệt độ thường.
- Ngoại quan: Chất lỏng trong suốt, không màu, mùi ngọt giống ether.
- Mật độ: 1.489 g/cm³ ở 25°C, nặng hơn nước.
- Điểm sôi: 61.15°C, dễ bay hơi ở nhiệt độ thường.
- Điểm nóng chảy: -63.5°C.
- Độ tan trong nước: Thấp, khoảng 8 g/L ở 20°C, nhưng tan tốt trong ethanol, ether, benzene, acetone.
- Áp suất hơi: 160 mm Hg ở 20°C, tạo hơi độc nhanh chóng.
- Chỉ số khúc xạ: 1.4459 ở 20°C.
- Độ nhớt: 0.563 cP ở 20°C.
Tính Chất Hóa Học Của Chloroform
Chloroform có công thức CHCl₃, khối lượng phân tử 119.37 g/mol, tính axit pKa 15.7, phân hủy dưới ánh sáng tạo phosgene, và bị oxy hóa thành trichloromethanol gây độc tính.
- Công thức phân tử: CHCl₃, khối lượng phân tử 119.37 g/mol.
- Tính axit: pKa 15.7 ở 20°C, có thể mất proton tạo dichlorocarbene (CCl₂) với base mạnh.
- Phản ứng: Phân hủy dưới ánh sáng hoặc nhiệt với oxy thành phosgene (COCl₂) và HCl; ổn định với ethanol làm chất ức chế.
- Tính oxy hóa: Bị oxy hóa bởi cytochrome P-450 thành trichloromethanol, dẫn đến độc tính.
- Tính phân cực: Có moment lưỡng cực 1.15 D, tan tốt chất hữu cơ không phân cực.
- Bền nhiệt: Phân hủy ở 450°C, không cháy tự nhiên nhưng hỗn hợp với chất dễ cháy có thể cháy.
Ứng Dụng Chính Của Chloroform
Chloroform chủ yếu dùng làm tiền chất sản xuất HCFC-22 và PTFE, chiếm phần lớn sản lượng toàn cầu khoảng 757 nghìn tấn năm 2024, dự kiến 1.02 triệu tấn năm 2035; dung môi trong lab và công nghiệp.
- Công nghiệp: Làm tiền chất sản xuất HCFC-22 (chất làm lạnh) và tetrafluoroethylene (PTFE, Teflon); chiếm phần lớn sản lượng toàn cầu.
- Dung môi: Hòa tan lipid, cao su, alkaloid, sáp, nhựa; dùng trong công thức thuốc trừ sâu, chất tẩy rửa, keo dán, sản xuất kháng sinh.
- Phòng thí nghiệm: Dung môi trong quang phổ NMR (deuterochloroform CDCl₃); tách chiết phenol-chloroform cho DNA/RNA; tạo dichlorocarbene trong phản ứng Reimer-Tiemann hoặc Kharasch.
- Khác: Làm chất hun trùng ngũ cốc, chất dập lửa (ít dùng nay); trong sản xuất giấy, dược phẩm làm dung môi.
Lưu Ý An Toàn Khi Sử Dụng Chloroform
Chloroform gây chóng mặt, tổn thương gan/thận, nghi gây ung thư (AML leukemia), liều chết trung bình 45 g; giới hạn OSHA PEL 50 ppm (ceiling), ACGIH TLV 10 ppm TWA.
- Rủi ro sức khỏe: Gây chóng mặt, buồn nôn, tổn thương gan/thận, hôn mê nếu hít cao; nghi gây ung thư gan/thận và leukemia; liều gây chết trung bình 45 g uống.
- Giới hạn phơi nhiễm: OSHA PEL 50 ppm (ceiling), ACGIH TLV 10 ppm TWA trong 8 giờ; IDLH 500 ppm.
- Xử lý: Sử dụng tủ hút hóa chất, mang găng nitrile, kính bảo hộ, áo lab; tránh hít, nuốt, tiếp xúc da.
- Xử lý sự cố: Nếu hít, di chuyển đến không khí sạch; da/mắt rửa nước 15 phút; nuốt không gây nôn, gọi cấp cứu ngay.
- Lưu trữ: Nơi mát, khô, thông gió, xa nguồn nhiệt/ánh sáng; dùng chất ổn định như ethanol để tránh tạo phosgene.
- Thải bỏ: Thu gom như chất thải nguy hại, không đổ cống; tuân thủ quy định địa phương.
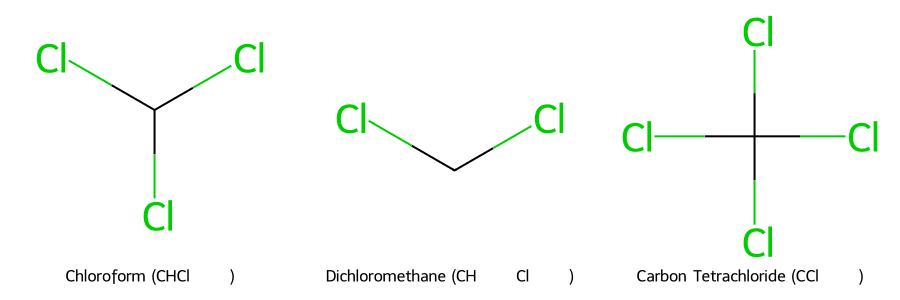
So Sánh Chloroform Với Các Dung Môi Tương Tự
Chloroform có điểm sôi 61°C, độc tính cao (gây ung thư), ứng dụng dung môi lab; so với dichloromethane (40°C, trung bình độc) và carbon tetrachloride (77°C, cao độc, phá ozone).
| Đặc điểm | Chloroform (CHCl₃) | Dichloromethane (CH₂Cl₂) | Carbon Tetrachloride (CCl₄) |
|---|---|---|---|
| Điểm sôi | 61°C | 40°C | 77°C |
| Độc tính | Cao, gây ung thư | Trung bình, gây chóng mặt | Cao, cấm dùng nhiều nơi |
| Ứng dụng chính | Dung môi lab, tiền chất PTFE | Dung môi sơn, tẩy rửa | Dung môi cũ, nay hạn chế |
| Độ tan nước | Thấp (8 g/L) | Trung bình (13 g/L) | Rất thấp (0.8 g/L) |
| Rủi ro môi trường | Tạo THM trong nước clo hóa | Bay hơi nhanh | Phá hủy ozone |
Câu Hỏi Thường Gặp Về Chloroform
Chloroform có độc, gây hại hệ thần kinh, gan, thận; dùng trong lab dưới tủ hút; thay thế an toàn như ethyl acetate hoặc dimethyl carbonate.
- Chloroform có độc không? Có, gây hại hệ thần kinh, gan, thận; tránh hít lâu dài.
- Chloroform dùng để làm gì trong lab? Dung môi tách chiết, NMR; xử lý cẩn thận dưới tủ hút.
- Làm thế nào xử lý nếu tiếp xúc? Rửa ngay, gọi cấp cứu nếu nặng; không gây nôn nếu nuốt.
- Chloroform có trong nước uống? Có thể hình thành từ clo hóa, giới hạn <100 μg/L.
- Có thay thế an toàn cho chloroform? Dùng ethyl acetate, dimethyl carbonate hoặc isopropanol cho tách chiết để giảm rủi ro.
Người kiểm duyệt nội dung
PGS.TS Đặng Hoàng Phú
Cố vấn chuyên môn cấp cao tại Hóa Chất Doanh Tín. Phó Giáo sư, Giảng viên Khoa Hóa học (ĐH KHTN ĐHQG-HCM) với hơn 10 năm kinh nghiệm nghiên cứu Hóa hữu cơ & Phổ nghiệm.
Xem hồ sơ năng lực & công bố khoa học →









