Kiến thức chuyên môn
Hợp Chất Vô Cơ: Phân Loại, Tính Chất & Ứng Dụng Công Nghiệp
Trong huyết mạch của mọi ngành công nghiệp hiện đại, từ sản xuất thép, dệt nhuộm đến xử lý nước thải, đều có sự hiện diện của các hợp chất vô cơ. Chúng không chỉ là những công thức trong sách giáo khoa mà còn là nền tảng vận hành sản xuất, quyết định chất lượng sản phẩm và hiệu quả chi phí.
Tại Hóa Chất Doanh Tín, chúng tôi hiểu rằng việc nắm vững kiến thức từ cơ bản đến chuyên sâu về các loại hóa chất này không chỉ là yêu cầu kỹ thuật mà còn là lợi thế cạnh tranh. Hãy cùng chúng tôi khám phá thế giới của hợp chất vô cơ qua lăng kính ứng dụng công nghiệp thực tiễn.

1. Hợp chất vô cơ được định nghĩa nền tảng là gì?
Về cơ bản, hợp chất vô cơ là bất kỳ hợp chất hóa học nào không chứa liên kết carbon-hydro (C-H). Đây là điểm khác biệt cốt lõi so với hợp chất hữu cơ.
Tuy nhiên, có một vài ngoại lệ quan trọng cần lưu ý trong công nghiệp, bao gồm:
- Các oxit của carbon (CO, CO₂)
- Axit cacbonic (H₂CO₃) và các muối cacbonat/hydrocarbonat (như Natri Cacbonat hay CaCO₃)
- Các muối xyanua (như Sodium Cyanide)
- Các carbide kim loại (như CaC₂)
Trong môi trường công nghiệp, hợp chất vô cơ là nguyên liệu thô, chất xúc tác, và tác nhân xử lý không thể thiếu, được tổng hợp với quy mô lớn để đáp ứng các tiêu chuẩn chất lượng khắt khe nhất, đảm bảo hiệu quả sản xuất tối ưu.
2. Hóa học vô cơ có mấy trụ cột phân loại chính và ứng dụng then chốt là gì?
Toàn bộ thế giới hợp chất vô cơ được phân loại thành bốn trụ cột chính: Oxit, Axit, Bazơ, và Muối. Mỗi nhóm này đều đóng một vai trò riêng biệt và không thể thay thế trong các ngành công nghiệp then chốt.
Việc hiểu rõ đặc tính và ứng dụng của từng nhóm giúp các doanh nghiệp lựa chọn đúng loại hóa chất, tối ưu hóa quy trình và nâng cao chất lượng sản phẩm cuối cùng.
Oxit là gì và ứng dụng trong ngành vật liệu xây dựng & gốm sứ ra sao?
Oxit là hợp chất của oxy với một nguyên tố khác, là thành phần chính của hầu hết các loại khoáng sản, đất đá và đóng vai trò nền tảng trong sản xuất vật liệu xây dựng, gốm sứ.
Oxit (ví dụ: Fe₂O₃, Al₂O₃, CaO) là các hợp chất cực kỳ phổ biến trong vỏ Trái Đất. Theo thống kê của ngành công nghiệp, ngành sản xuất xi măng toàn cầu tiêu thụ hàng tỷ tấn vôi sống (CaO) mỗi năm.
Ứng dụng công nghiệp chính: Sản xuất xi măng, luyện gang thép từ quặng oxit sắt, sản xuất gốm sứ, và làm chất tạo màu trắng phổ biến (TiO₂).
Axit có vai trò động lực như thế nào trong ngành luyện kim và xử lý bề mặt?
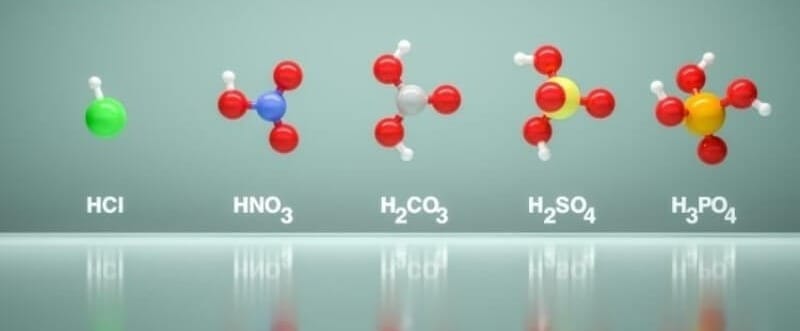
Axit là hợp chất tạo ra ion H⁺ khi hòa tan trong nước, với độ mạnh quyết định khả năng ăn mòn và phản ứng, trở thành động lực không thể thiếu cho ngành luyện kim và xử lý bề mặt kim loại.
Các loại axit mạnh (ví dụ: H₂SO₄, HCl, HNO₃) là hóa chất nền tảng trong nhiều quy trình công nghiệp. Ngành công nghiệp thép toàn cầu sử dụng hàng triệu tấn HCl mỗi năm chỉ cho công đoạn tẩy rỉ sét trước khi mạ.
Ứng dụng công nghiệp chính: Tẩy rỉ sét thép (HCl), sản xuất phân bón (Supephotphat từ H₂SO₄), sản xuất thuốc nổ, và xi mạ kim loại.
Tại sao Bazơ được coi là trái tim của ngành sản xuất giấy và chất tẩy rửa?
Bazơ là hợp chất tạo ra ion OH⁻ trong nước, có khả năng trung hòa axit và phân hủy chất béo, khiến chúng trở thành hóa chất cốt lõi trong quy trình sản xuất giấy và mọi loại chất tẩy rửa.
Bazơ (ví dụ: NaOH, Ca(OH)₂, KOH) thường có tính nhờn và là tác nhân làm sạch hiệu quả. Ngành công nghiệp giấy và bột giấy là một trong những ngành tiêu thụ NaOH lớn nhất thế giới, sử dụng hóa chất này để phân hủy lignin và tách sợi cellulose.
Ứng dụng công nghiệp chính: Sản xuất xà phòng và chất tẩy rửa, sản xuất giấy (NaOH), xử lý nước thải (vôi tôi Ca(OH)₂ để điều chỉnh độ pH).
Muối có phải là hóa chất không thể thiếu trong nông nghiệp và xử lý nước không?
Chắc chắn là vậy. Muối, được tạo thành từ phản ứng trung hòa, là thành phần không thể thiếu trong sản xuất phân bón, cung cấp dinh dưỡng cho cây trồng và là tác nhân keo tụ chính trong ngành xử lý nước.
Muối (ví dụ: NaCl, CuSO₄, NaNO₃) có hàng ngàn ứng dụng khác nhau. Thị trường phân bón toàn cầu, dự kiến đạt giá trị hơn 200 tỷ USD vào năm 2025, phụ thuộc gần như hoàn toàn vào các loại muối vô cơ như muối nitrat, photphat và kali.
Ứng dụng công nghiệp chính: Xử lý nước (phèn nhôm, PAC), sản xuất phân bón, bảo quản thực phẩm (NaCl), và thuốc trừ sâu (CuSO₄).
Bảng so sánh nhanh: PAC và Phèn Nhôm trong xử lý nước
| Tiêu Chí | Poly Aluminium Chloride (PAC) | Phèn Nhôm (Al₂(SO₄)₃) |
|---|---|---|
| Hiệu quả keo tụ | Mạnh hơn, tốc độ nhanh hơn | Trung bình |
| Khoảng pH hoạt động | Rộng (5.0 – 9.0) | Hẹp (6.5 – 7.5) |
| Lượng bùn thải | Ít hơn | Nhiều hơn |
| Chi phí | Cao hơn | Thấp hơn |
3. Những hợp chất vô cơ công nghiệp nào quan trọng nhất tại Việt Nam?
Các hợp chất vô cơ công nghiệp được xem là xương sống của nền sản xuất tại Việt Nam bao gồm Axit Sunfuric (H₂SO₄), Natri Hydroxit (NaOH), Axit Clohydric (HCl), và các hợp chất gốc Clo như Javen (NaClO) và Chlorine (Cl₂).
Sự ổn định nguồn cung và chất lượng của các hóa chất này ảnh hưởng trực tiếp đến năng lực cạnh tranh của nhiều ngành kinh tế trọng điểm của quốc gia.
- Axit Sunfuric (H₂SO₄): Được mệnh danh là “vua của các loại hóa chất”, H₂SO₄ được sử dụng rộng rãi trong sản xuất phân bón, lọc dầu, xử lý nước thải và sản xuất ắc quy.
- Natri Hydroxit (NaOH – Xút): Là hóa chất nền tảng cho ngành công nghiệp giấy, dệt nhuộm, sản xuất xà phòng, và khai thác dầu mỏ. Độ tinh khiết của NaOH ảnh hưởng trực tiếp đến chất lượng sản phẩm cuối cùng.
- Axit Clohydric (HCl): Chủ yếu được dùng để tẩy rỉ thép trước khi mạ, xử lý da trong ngành thuộc da, và sản xuất các hợp chất hữu cơ khác.
- Hypochlorite (Javen – NaClO) & Chlorine (Cl₂): Là các chuyên gia khử trùng, được ứng dụng trong xử lý nước cấp, nước thải, và làm chất tẩy trắng trong ngành dệt may.

Case Study Thực Tế: Tối Ưu Hóa Chi Phí Xử Lý Nước Thải Cho Nhà Máy Dệt Nhuộm
Một đối tác của chúng tôi trong ngành dệt nhuộm tại Bình Dương đã gặp vấn đề với hệ thống xử lý nước thải hoạt động kém hiệu quả, chi phí phèn nhôm cao và lượng bùn thải lớn. Sau khi khảo sát, đội ngũ kỹ thuật của Doanh Tín đã tư vấn họ chuyển sang sử dụng PAC với liều lượng tối ưu.
Kết quả: Giảm 30% lượng hóa chất sử dụng, giảm 40% lượng bùn thải, và nước sau xử lý đạt tiêu chuẩn loại A, giúp doanh nghiệp tiết kiệm hàng trăm triệu đồng mỗi năm.
4. Nguyên tắc vàng về an toàn và tuân thủ khi sử dụng hóa chất vô cơ là gì?
Nguyên tắc vàng là tuân thủ nghiêm ngặt các quy định an toàn, đặc biệt là thông tin trên Bảng Dữ Liệu An Toàn (SDS), các quy định của pháp luật Việt Nam (Nghị định 113/2017/NĐ-CP), và luôn sử dụng đầy đủ Trang bị Bảo hộ Cá nhân (PPE).
Làm việc với hóa chất công nghiệp đòi hỏi sự tuân thủ tuyệt đối các quy định an toàn để bảo vệ con người, tài sản và môi trường. Theo báo cáo gần đây, việc áp dụng đúng các quy trình an toàn có thể giảm tới 90% các tai nạn lao động liên quan đến hóa chất.
- Tầm quan trọng của SDS (Safety Data Sheet): Mỗi hóa chất đều phải đi kèm Bảng Dữ Liệu An Toàn, cung cấp thông tin chi tiết về đặc tính, tác hại của hóa chất, và biện pháp xử lý sự cố.
- Tuân thủ quy định Việt Nam: Nghị định 113/2017/NĐ-CP của Chính phủ quy định chi tiết về Luật Hóa chất, bao gồm các yêu cầu về bảo quản hóa chất và ghi nhãn hóa chất theo GHS.
- Trang bị Bảo hộ Cá nhân (PPE): Luôn sử dụng đầy đủ găng tay, kính mắt, quần áo bảo hộ phù hợp khi tiếp xúc với hóa chất, đặc biệt là axit và bazơ mạnh.

Tuân thủ nghiêm ngặt quy định an toàn lao động là ưu tiên hàng đầu khi làm việc với hóa chất.
Mẹo Chuyên Gia Từ Nguyễn Thị Mỹ Linh
“Một quy tắc an toàn cơ bản nhưng cực kỳ quan trọng: Luôn luôn cho từ từ axit vào nước, tuyệt đối không làm ngược lại. Phản ứng giữa axit đặc và nước là một phản ứng tỏa nhiệt mạnh, có thể gây sôi đột ngột và bắn hóa chất nguy hiểm.”
5. Làm thế nào để lựa chọn nhà cung cấp hóa chất vô cơ uy tín và cam kết của Doanh Tín là gì?
Để lựa chọn nhà cung cấp uy tín, cần dựa trên các tiêu chí về chất lượng, độ tinh khiết, dịch vụ tư vấn kỹ thuật chuyên sâu và cam kết về nguồn gốc sản phẩm. Hóa Chất Doanh Tín cam kết đáp ứng đầy đủ và vượt trội các tiêu chí này.
Chất lượng của hóa chất đầu vào quyết định sự thành bại của cả một quy trình sản xuất. Một nhà cung cấp uy tín không chỉ bán sản phẩm, mà còn mang lại giải pháp toàn diện.
- Tại sao Chất lượng và Độ tinh khiết quan trọng? Tạp chất trong hóa chất có thể gây ra các phản ứng phụ không mong muốn, làm giảm hiệu suất, hư hỏng thiết bị và ảnh hưởng đến chất lượng sản phẩm. Việc sử dụng chất tinh khiết là yêu cầu bắt buộc trong nhiều ngành.
- Dịch vụ Tư vấn Kỹ thuật Chuyên sâu: Tại Hóa Chất Doanh Tín, đội ngũ chuyên gia của chúng tôi luôn sẵn sàng tư vấn để bạn chọn đúng loại hóa chất, đúng nồng độ vàเกรด tinh khiết cho ứng dụng cụ thể của mình.
- Cam kết Nguồn gốc và Sự ổn định: Chúng tôi đảm bảo nguồn cung ổn định, sản phẩm có nguồn gốc xuất xứ rõ ràng, đầy đủ chứng từ COA (Certificate of Analysis).
Trích Dẫn Từ Chuyên Gia
“Từ kinh nghiệm của tôi tại Doanh Tín, việc lựa chọn sai nồng độ hoặc nhận phải lô xút có tạp chất sắt cao có thể làm hỏng cả một lô vải nhuộm màu sáng. Đó là lý do tư vấn kỹ thuật chuyên sâu và kiểm soát chất lượng đầu vào (COA) luôn là ưu tiên hàng đầu của chúng tôi.”
– Nguyễn Thị Mỹ Linh, Chuyên gia Kỹ thuật, Hóa Chất Doanh Tín.
Nhận ngay “Checklist 5 Tiêu Chí Vàng Để Lựa Chọn Nhà Cung Cấp Hóa Chất Công Nghiệp” để đảm bảo bạn luôn có được đối tác tốt nhất.
6. Những câu hỏi thường gặp về hóa chất vô cơ là gì?
1. Sự khác biệt giữa hóa chất công nghiệp và hóa chất tinh khiết (phân tích) là gì?
Hóa chất công nghiệp được sản xuất với số lượng lớn, đáp ứng tiêu chuẩn cho sản xuất nhưng có thể chứa một lượng nhỏ tạp chất. Hóa chất tinh khiết (เกรด phân tích), như các sản phẩm của Sigma-Aldrich, có độ tinh khiết cực cao (thường >99.9%), dùng cho nghiên cứu, phân tích trong phòng thí nghiệm và có giá thành cao hơn nhiều.
2. Hóa Chất Doanh Tín có hỗ trợ kỹ thuật khi chúng tôi gặp sự cố không?
Chắc chắn có. Đội ngũ kỹ thuật của chúng tôi luôn sẵn sàng hỗ trợ khách hàng từ việc lựa chọn sản phẩm đến việc tối ưu hóa quy trình sử dụng. Bạn có thể xem thêm thông tin về đội ngũ chuyên gia của chúng tôi tại trang tuyển dụng.
3. Thời gian giao hàng cho khu vực Bình Dương, Đồng Nai, TP.HCM là bao lâu?
Chúng tôi cam kết giao hàng trong vòng 24-48 giờ đối với các mặt hàng có sẵn tại kho cho các khu vực công nghiệp trọng điểm phía Nam. Toàn bộ sản phẩm có sẵn đều được niêm yết tại cửa hàng trực tuyến của chúng tôi.
7. Tại sao việc hiểu rõ về hợp chất vô cơ lại quan trọng và vai trò của Hóa Chất Doanh Tín là gì?
Hiểu rõ về hợp chất vô cơ là chìa khóa để tối ưu hóa sản xuất, đảm bảo an toàn và nâng cao năng lực cạnh tranh. Vai trò của Hóa Chất Doanh Tín là trở thành đối tác tin cậy, cung cấp sản phẩm chất lượng và giải pháp kỹ thuật chuyên nghiệp.
Hóa Chất Doanh Tín tự hào là đối tác đồng hành cùng các doanh nghiệp Việt Nam, không chỉ cung cấp các sản phẩm chất lượng cao mà còn mang đến các giải pháp kỹ thuật giúp khách hàng phát triển bền vững.
Bạn cần tư vấn giải pháp hóa chất cho nhà máy của mình?
Bạn muốn nhận báo giá cạnh tranh cho H₂SO₄, NaOH, PAC?
Tuyên bố miễn trừ trách nhiệm: Mọi thông tin trong bài viết chỉ mang tính chất tham khảo. Luôn luôn tham khảo Bảng Dữ Liệu An Toàn (SDS) của sản phẩm và tuân thủ các quy định pháp luật hiện hành khi làm việc với hóa chất.
Người kiểm duyệt nội dung
PGS.TS Đặng Hoàng Phú
Cố vấn chuyên môn cấp cao tại Hóa Chất Doanh Tín. Phó Giáo sư, Giảng viên Khoa Hóa học (ĐH KHTN ĐHQG-HCM) với hơn 10 năm kinh nghiệm nghiên cứu Hóa hữu cơ & Phổ nghiệm.
Xem hồ sơ năng lực & công bố khoa học →









