Kiến thức chuyên môn
Amoniac (NH3) là gì? Chuyên Sâu Tính Chất & Ứng Dụng An Toàn
Amoniac (NH3) là một trong những hợp chất vô cơ được sản xuất nhiều nhất trên thế giới, đóng vai trò nền tảng cho nông nghiệp và vô số ngành công nghiệp. Tuy nhiên, sự phổ biến của nó đi kèm với những yêu cầu nghiêm ngặt về kiến thức kỹ thuật và an toàn vận hành.
Tại Hóa Chất Doanh Tín, chúng tôi hiểu rằng việc cung cấp amoniac không chỉ là bán một sản phẩm, mà là trao một giải pháp an toàn và hiệu quả. Bài viết này sẽ đi sâu vào bản chất của amoniac, giúp bạn hiểu rõ từ cấu trúc phân tử đến các ứng dụng thực tiễn, và quan trọng nhất, là cách làm chủ hóa chất quan trọng này một cách an toàn theo đúng tiêu chuẩn Việt Nam.
1. Amoniac (NH3) có những đặc điểm tổng quan nào?
Amoniac (NH₃) là một hợp chất khí không màu của nitơ và hydro, có mùi khai nồng, nhẹ hơn không khí và có cấu trúc phân tử hình chóp tam giác, quyết định các tính chất hóa học đặc trưng của nó.
Amoniac, còn được viết là a-mô-ni-ắc, là một hợp chất của nitơ và hydro với công thức hóa học là NH₃. Ở điều kiện tiêu chuẩn, nó là một chất khí không màu, có mùi khai nồng đặc trưng rất dễ nhận biết, nhẹ hơn không khí.
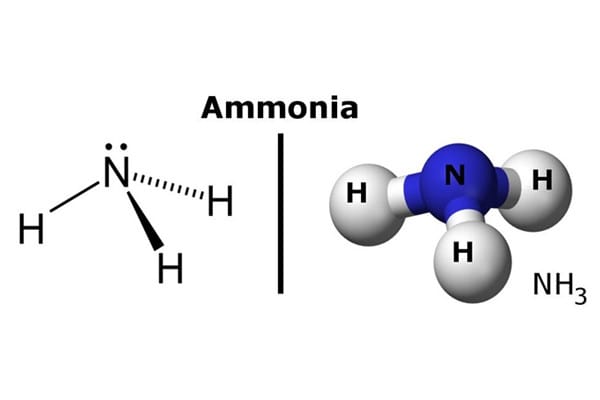
Phân tử NH₃ có cấu trúc chóp tam giác, được hình thành bởi các liên kết cộng hóa trị giữa nguyên tử Nitơ ở đỉnh và ba nguyên tử Hydro ở đáy. Chính cặp electron tự do (chưa liên kết) trên nguyên tử Nitơ đã tạo nên những tính chất hóa học đặc trưng và làm nên giá trị của amoniac.
2. Làm thế nào để phân biệt Amoniac Khan và Dung dịch Amoniac?
Amoniac Khan là NH₃ nguyên chất (>99.5%) ở dạng lỏng dưới áp suất cao, dùng làm môi chất lạnh và sản xuất hóa chất. Dung dịch Amoniac là NH₃ hòa tan trong nước (20-35%), dùng để điều chỉnh pH và làm chất tẩy rửa.
Trên thị trường công nghiệp, amoniac tồn tại ở hai dạng thương mại chính: Amoniac khan và Dung dịch Amoniac. Việc nhầm lẫn giữa hai loại này có thể dẫn đến hậu quả nghiêm trọng về hiệu quả sản xuất và an toàn lao động.
2.1. Amoniac Khan (Anhydrous Ammonia) là gì và có đặc điểm ra sao?
Đây là amoniac nguyên chất (>99.5%), không chứa nước, được nén thành dạng lỏng dưới áp suất cao và sôi ở -33.34°C khi giảm áp, dùng trong công nghiệp lạnh và sản xuất hóa chất.
- Bản chất: Là NH₃ ở dạng nguyên chất (>99.5%), hoàn toàn không chứa nước.
- Trạng thái: Là khí ở điều kiện thường, được nén thành dạng lỏng trong các bình chịu áp suất cao. Khi giảm áp, nó sôi và hóa hơi tức thì ở -33.34°C, thu nhiệt mạnh từ môi trường xung quanh. Đây chính là nguyên lý của ứng dụng làm lạnh.
- Tên gọi khác: Amoniac lỏng, Khí amoniac hóa lỏng, Môi chất lạnh R717.
- Ứng dụng chính:
- Công nghiệp lạnh: Là môi chất lạnh R717 trong các hệ thống cấp đông, kho lạnh, nhà máy bia, nhà máy chế biến thủy hải sản.
- Sản xuất hóa chất: Nguyên liệu cốt lõi để sản xuất axit nitric (HNO₃), phân urê, amoni nitrat (AN).
- Xử lý nhiệt luyện kim loại: Dùng trong quá trình thấm nitơ để làm cứng bề mặt thép.
2.2. Dung Dịch Amoniac (Aqua Ammonia) là gì và ứng dụng như thế nào?
Đây là dung dịch của khí NH₃ hòa tan trong nước, tạo thành amoni hydroxit (NH₄OH) nồng độ 20-35%, có tính bazơ yếu và được dùng chủ yếu để xử lý nước, dệt may, và làm chất tẩy rửa.
- Bản chất: Là khí NH₃ được hòa tan trong nước. Phản ứng tạo ra amoni hydroxit (NH₄OH), một dung dịch có tính bazơ yếu.
- Nồng độ: Thường có nồng độ từ 20% – 35%.
- Tên gọi khác: Nước amoniac, Amoni hydroxit.
- Ứng dụng chính:
- Xử lý nước thải: Dùng để điều chỉnh và nâng độ pH, kết hợp với các hóa chất xử lý nước khác như PAC Vàng Chanh.
- Ngành dệt may: Điều chỉnh pH trong quá trình nhuộm và xử lý vải.
- Sản xuất chất tẩy rửa: Là thành phần trong nước lau kính và nhiều chất tẩy rửa đa năng (như Javen).
- Công nghiệp cao su: Dùng làm chất chống đông tụ mủ cao su.
2.3. Lời khuyên của chuyên gia khi lựa chọn amoniac là gì?
Luôn xác định rõ mục đích sử dụng cuối cùng để lựa chọn đúng loại amoniac (khan hay dung dịch), tránh lãng phí và các rủi ro an toàn nghiêm trọng do sử dụng sai thiết bị chuyên dụng.
Chia sẻ từ Nguyễn Thị Mỹ Linh, chuyên gia kỹ thuật tại Hóa Chất Doanh Tín:
“Một sai lầm phổ biến mà chúng tôi thường thấy là khách hàng yêu cầu ‘amoniac lỏng’ nhưng mục đích lại là để trung hòa axit trong hệ thống xử lý nước thải. Trong trường hợp này, sản phẩm họ thực sự cần là Dung dịch Amoniac, không phải Amoniac Khan (thường cũng được gọi là amoniac lỏng). Sử dụng sai loại không chỉ gây lãng phí chi phí mà còn tiềm ẩn rủi ro an toàn cực lớn do amoniac khan yêu cầu thiết bị chịu áp suất cao chuyên dụng. Luôn trao đổi rõ với nhà cung cấp về mục đích sử dụng cuối cùng của bạn để nhận được tư vấn chính xác nhất.”
3. Amoniac có những tính chất hóa học đặc trưng nào?
Amoniac có ba tính chất hóa học cốt lõi: tính bazơ yếu (do cặp electron tự do), tính khử mạnh ở nhiệt độ cao, và khả năng tạo phức với ion kim loại, từ đó quyết định các ứng dụng đa dạng của nó.
Hiểu rõ tính chất hóa học là chìa khóa để khai thác tối đa tiềm năng của amoniac.
3.1. Tại sao Amoniac có tính bazơ yếu?
Trong dung dịch nước, phân tử NH₃ nhận một proton (H⁺) từ nước, tạo ra ion OH⁻, làm dung dịch có tính kiềm. Đây là tính chất giúp amoniac trung hòa axit và sản xuất phân đạm.
Trong dung dịch nước, amoniac nhận một proton (H⁺) từ nước, thể hiện tính bazơ:
NH₃ + H₂O ⇌ NH₄⁺ + OH⁻
Phản ứng này tạo ra ion OH⁻, làm cho dung dịch có tính kiềm, có khả năng làm quỳ tím hóa xanh hoặc phenolphtalein hóa hồng.
Ứng dụng thực tế:
- Trung hòa axit: Đây là một ví dụ điển hình của phản ứng trung hòa, được dùng để xử lý axit dư trong nước thải công nghiệp.
- Sản xuất phân đạm: Tác dụng với các axit mạnh như axit sunfuric (H₂SO₄) để tạo ra các loại phân bón quan trọng như Amoni sunfat ((NH₄)₂SO₄) hay Amoni nitrat (NH₄NO₃).
2NH₃ + H₂SO₄ → (NH₄)₂SO₄
3.2. Tính khử mạnh của Amoniac biểu hiện như thế nào?
Ở nhiệt độ cao và có xúc tác, amoniac bị oxy hóa, trong đó số oxy hóa của Nitơ tăng từ -3 lên các mức cao hơn. Phản ứng này là nền tảng cho quy trình sản xuất Axit Nitric.
Ở nhiệt độ cao và có chất xúc tác, amoniac có thể bị oxy hóa bởi các chất oxy hóa, thể hiện tính khử. Số oxy hóa của Nitơ tăng từ -3 lên các mức cao hơn.
Ứng dụng thực tế (Quan trọng nhất):
- Sản xuất Axit Nitric (Quy trình Ostwald): Đây là phản ứng nền tảng để sản xuất axit nitric, nguyên liệu cho thuốc nổ và phân bón.
4NH₃ + 5O₂ → (xúc tác 850-900°C, Pt) → 4NO + 6H₂O
3.3. Amoniac có khả năng tạo phức chất không?
Có, dung dịch amoniac có khả năng hòa tan các hydroxit hoặc muối ít tan của một số kim loại như đồng (Cu), bạc (Ag), kẽm (Zn) để tạo thành các ion phức tan, ứng dụng trong luyện kim và phân tích hóa học.
Dung dịch amoniac có khả năng hòa tan hydroxit hoặc muối ít tan của một số kim loại (Ag, Cu, Zn) bằng cách tạo ra các ion phức.
Ứng dụng thực tế:
- Luyện kim & Mạ điện: Dùng để chiết tách và tinh chế kim loại.
- Phân tích hóa học: Dùng làm thuốc thử để nhận biết một số ion kim loại.
Cu(OH)₂ + 4NH₃ → [Cu(NH₃)₄](OH)₂ (Phức chất màu xanh thẫm)
4. Các ứng dụng công nghiệp trọng điểm của Amoniac là gì?
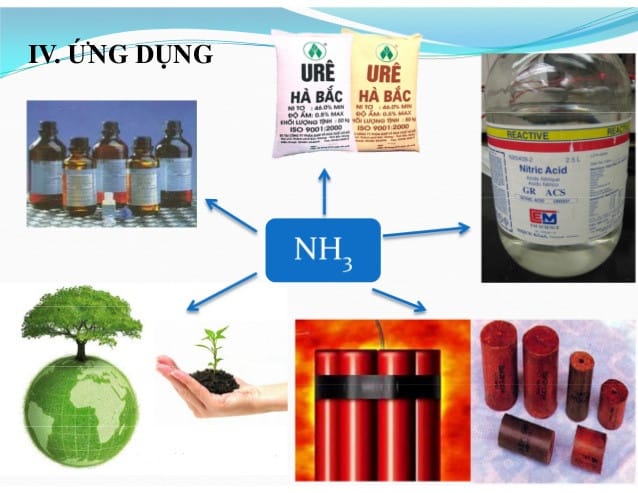
Amoniac chủ yếu được dùng để sản xuất phân bón (chiếm ~83%), làm môi chất lạnh (R717), xử lý khí thải, trong ngành dệt nhuộm, sản xuất chất nổ và xử lý bề mặt gỗ.
Từ những tính chất hóa học trên, amoniac đã trở thành hóa chất không thể thiếu trong nhiều lĩnh vực.
- Sản xuất Phân bón (chiếm ~83%): Là nguồn cung cấp đạm thiết yếu cho cây trồng. Amoniac được dùng để sản xuất urê, amoni sunfat (SA), amoni nitrat (AN), và các loại phân lân như supephotphat.
- Công nghiệp Lạnh: Amoniac khan (R717) là một môi chất lạnh hiệu quả và thân thiện với môi trường (Chỉ số GWP = 0, ODP = 0), được ưa chuộng trong các hệ thống lạnh công nghiệp quy mô lớn.
- Ngành Dệt Nhuộm: Dung dịch amoniac được dùng để làm sạch len, xử lý sợi bông (mercerizing) và làm chất xúc tác, điều chỉnh pH trong quá trình nhuộm.
- Xử lý Khí thải: Amoniac được sử dụng trong các hệ thống khử NOx chọn lọc như tháp hấp thụ (scrubber) để chuyển đổi các oxit nitơ độc hại trong khí thải nhà máy nhiệt điện thành khí nitơ và hơi nước vô hại.
- Sản xuất Thuốc và Chất nổ: Là tiền chất để sản xuất axit nitric, từ đó sản xuất ra nitroglycerin và TNT.
- Công nghiệp Gỗ: Dùng để xử lý bề mặt gỗ, làm sậm màu gỗ sồi một cách tự nhiên mà không cần dùng thuốc nhuộm.
5. Cần tuân thủ những tiêu chuẩn an toàn nào khi sử dụng Amoniac?
Phải tuân thủ nghiêm ngặt các quy định pháp luật Việt Nam như Nghị định 42/2020/NĐ-CP, TCVN 5507:2002, và hệ thống ghi nhãn GHS để đảm bảo an toàn tuyệt đối trong vận chuyển, lưu trữ và sử dụng.
Amoniac cực kỳ hữu ích nhưng cũng tiềm ẩn rủi ro cao. Việc tuân thủ quy định pháp luật là yêu cầu bắt buộc. Mọi hoạt động của chúng tôi đều tuân thủ nghiêm ngặt các văn bản pháp lý hiện hành và luôn cập nhật các điểm mới của Luật Hóa chất.
- Nghị định 42/2020/NĐ-CP: Quy định về danh mục hàng hóa nguy hiểm và vận chuyển hàng hóa nguy hiểm.
- TCVN 5507:2002: Quy phạm kỹ thuật an toàn trong sản xuất, kinh doanh, sử dụng, bảo quản và vận chuyển hóa chất nguy hiểm.
- Hệ thống GHS: Việc ghi nhãn hóa chất theo GHS là tiêu chuẩn bắt buộc để nhận diện rõ ràng các mối nguy.
5.1. Những rủi ro chính khi tiếp xúc với Amoniac là gì?
Các rủi ro chính bao gồm tổn thương đường hô hấp nghiêm trọng khi hít phải, bỏng hóa học (với dung dịch) hoặc bỏng lạnh (với amoniac khan) khi tiếp xúc da/mắt, và nguy cơ cháy nổ ở nồng độ cao trong không khí.
- Đường hô hấp: Hít phải khí NH₃ ở nồng độ cao gây bỏng niêm mạc, phù phổi cấp, có thể dẫn đến tử vong. Ngưỡng nguy hiểm tức thì đến tính mạng (IDLH) là 300 ppm.
- Tiếp xúc da/mắt: Dung dịch amoniac gây bỏng hóa học nặng. Amoniac khan hóa lỏng khi tiếp xúc với da sẽ gây bỏng lạnh cực kỳ nghiêm trọng do bay hơi nhanh và thu nhiệt.
- Cháy nổ: Mặc dù khó bắt lửa, hỗn hợp khí amoniac (16-25% trong không khí) có thể gây nổ nếu có nguồn đánh lửa.
5.2. Cần thực hiện các bước sơ cứu khẩn cấp nào khi gặp sự cố?
Ngay lập tức đưa nạn nhân đến nơi thoáng khí, cởi bỏ quần áo nhiễm bẩn, rửa vùng da/mắt bị ảnh hưởng bằng nước sạch liên tục trong ít nhất 20 phút và gọi cấp cứu 115.
- Khi hít phải: Đưa ngay nạn nhân đến nơi thoáng khí. Giữ ấm, đặt ở tư thế nửa ngồi và gọi cấp cứu 115.
- Khi dính vào da: Cởi bỏ quần áo bị nhiễm bẩn. Rửa vùng da dưới vòi nước sạch liên tục trong ít nhất 20 phút. Tuyệt đối không chà xát vùng da bị bỏng lạnh.
- Khi dính vào mắt: Rửa mắt ngay lập tức bằng dòng nước sạch trong ít nhất 20 phút, giữ mí mắt mở rộng. Đưa đến cơ sở y tế chuyên khoa mắt gần nhất.
Tuyên bố miễn trừ trách nhiệm: Thông tin sơ cứu trên chỉ mang tính tham khảo ban đầu. Luôn ưu tiên gọi cấp cứu y tế chuyên nghiệp (115) và tuân theo hướng dẫn của họ trong mọi tình huống.

5.3. Case Study: Giải pháp Amoniac của Doanh Tín đã mang lại hiệu quả thực tế ra sao?
Doanh Tín đã tư vấn và cung cấp Amoniac Khan (R717) thay thế hệ thống lạnh R22 cũ cho một nhà máy thủy sản, giúp tăng hiệu quả 15%, giảm chi phí năng lượng và đảm bảo tuân thủ tiêu chuẩn môi trường.
- Thách thức: Một nhà máy chế biến thủy sản gặp sự cố rò rỉ hệ thống lạnh R22 cũ, ảnh hưởng đến sản xuất và không đáp ứng tiêu chuẩn môi trường mới về các hợp chất CFC.
- Giải pháp: Hóa Chất Doanh Tín đã tư vấn và cung cấp Amoniac Khan (R717) để chuyển đổi sang hệ thống lạnh mới. Chúng tôi cũng phối hợp tổ chức buổi tập huấn an toàn vận hành và ứng phó sự cố cho toàn bộ đội ngũ kỹ thuật của nhà máy.
- Kết quả: Hệ thống mới hoạt động hiệu quả hơn 15%, chi phí năng lượng giảm, và nhà máy hoàn toàn tuân thủ các quy định về môi trường. Dự án này khẳng định năng lực của Doanh Tín không chỉ là cung cấp hóa chất mà còn là đồng hành cùng giải pháp toàn diện cho khách hàng.
6. Amoniac được điều chế trong công nghiệp như thế nào?
Gần như toàn bộ amoniac công nghiệp được sản xuất qua quy trình Haber-Bosch, tổng hợp từ khí nitơ và hydro dưới nhiệt độ (400–450°C), áp suất cực cao (150–250 bar) và xúc tác sắt (Fe).
Ngày nay, gần như toàn bộ amoniac trên thế giới được sản xuất theo quy trình Haber-Bosch. Đây là một phát minh vĩ đại, giúp chuyển hóa nitơ trơ trong không khí thành dạng đạm mà cây trồng có thể hấp thụ.
- Phương trình phản ứng:
N₂(k) + 3H₂(k) ⇌ 2NH₃(k), ΔH = −92.4 kJ/mol - Điều kiện tối ưu:
- Nhiệt độ: 400 – 450°C.
- Áp suất: 150 – 250 bar (rất cao).
- Chất xúc tác: Sắt (Fe) được hoạt hóa với K₂O, Al₂O₃.
Hỗn hợp khí N₂ và H₂ được nén ở áp suất cực cao và đưa qua tháp tổng hợp chứa chất xúc tác, nơi phản ứng tạo ra amoniac diễn ra. Hỗn hợp khí sau đó được làm lạnh để hóa lỏng và thu hồi amoniac. Để tăng hiệu suất, khí NH₃ thường được làm khô bằng các chất làm khô hiệu quả.
7. Các câu hỏi thường gặp (FAQ) về Amoniac
Amoniac có mùi gì và tại sao?
Amoniac có mùi khai nồng, hắc rất đặc trưng. Mùi này là một cơ chế cảnh báo tự nhiên hiệu quả, giúp con người có thể phát hiện sự hiện diện của nó trong không khí ở nồng độ rất thấp, trước cả khi đạt đến ngưỡng gây nguy hiểm.
Nồng độ amoniac bao nhiêu là nguy hiểm?
Theo Viện An toàn và Sức khỏe Nghề nghiệp Quốc gia Hoa Kỳ (NIOSH), nồng độ 300 ppm được coi là Nguy hiểm Ngay lập tức đến Tính mạng và Sức khỏe (IDLH). Tiếp xúc ngắn ở nồng độ này có thể gây tổn thương phổi vĩnh viễn hoặc tử vong. Giới hạn tiếp xúc an toàn trong 8 giờ làm việc thường là 25 ppm.
Làm thế nào để lưu trữ dung dịch amoniac tại nhà máy?
Dung dịch amoniac cần được chứa trong các bồn nhựa (HDPE, composite) hoặc thép không gỉ, tuân thủ các nguyên tắc chung về bảo quản hóa chất an toàn: đặt ở nơi khô ráo, thoáng mát, tránh ánh nắng trực tiếp, có biển báo nguy hiểm, xa nguồn nhiệt và các axit mạnh.
Làm thế nào để xử lý mùi amoniac nhẹ trong khu vực làm việc?
Đối với mùi nhẹ, ưu tiên hàng đầu là tăng cường thông gió bằng cách mở cửa sổ, bật quạt hút. Có thể sử dụng các dung dịch có tính axit nhẹ như giấm pha loãng hoặc nước chanh để lau các bề mặt bị bám mùi. Tuy nhiên, nếu mùi nồng và kéo dài, đó có thể là dấu hiệu rò rỉ và cần thực hiện quy trình ứng phó sự cố ngay lập tức.
Amoniac “xanh” (Green Ammonia) là gì?
Đây là một xu hướng của ngành hóa chất năm 2024-2025. Amoniac “xanh” được sản xuất từ hydro tạo ra bằng phương pháp điện phân nước sử dụng năng lượng tái tạo (điện gió, mặt trời). Quá trình này không phát thải carbon, hứa hẹn một tương lai sản xuất phân bón bền vững.
8. Có những tài liệu và công cụ hữu ích nào về Amoniac?
Bạn có thể tải về hướng dẫn sơ cứu khẩn cấp dưới dạng PDF và sử dụng công cụ tính toán nồng độ dung dịch trực tuyến để hỗ trợ quá trình làm việc an toàn và hiệu quả hơn.
[PDF] Tải về Hướng dẫn Sơ cứu Khẩn cấp khi tiếp xúc với Amoniac
Mô tả: Tài liệu A4 dễ in, có thể dán tại nơi làm việc, tóm tắt các bước sơ cứu quan trọng nhất.
[Công cụ] Ước tính Nồng độ Dung dịch Amoniac
Mô tả: Một công cụ tính toán đơn giản giúp bạn pha loãng dung dịch amoniac từ nồng độ cao xuống nồng độ mong muốn.
9. Kết luận về tầm quan trọng của Amoniac?
Amoniac là hóa chất nền tảng cho nông nghiệp và công nghiệp hiện đại. Việc hiểu rõ các dạng, tính chất và tuân thủ tuyệt đối quy trình an toàn là yếu tố sống còn để khai thác hóa chất này một cách hiệu quả và bền vững.
Amoniac không chỉ là một hóa chất cơ bản, nó là mạch máu của nền nông nghiệp hiện đại và là một công cụ không thể thiếu trong nhiều quy trình công nghiệp. Việc hiểu rõ sự khác biệt giữa amoniac khan và dung dịch, nắm vững tính chất hóa học và tuân thủ tuyệt đối các quy trình an toàn là yếu-tố-sống-còn để khai thác hiệu quả và bền vững hóa chất này.
Bạn cần tư vấn kỹ thuật chuyên sâu hơn cho ứng dụng của mình? Hay đang tìm kiếm một nhà cung cấp amoniac uy tín, có đủ năng lực vận chuyển an toàn trên toàn quốc?
Bài viết được biên soạn bởi Nguyễn Thị Mỹ Linh, Chuyên gia Kỹ thuật Hóa chất với 10 năm kinh nghiệm trong ngành, và được duyệt bởi Ban Cố vấn Kỹ thuật của Hóa Chất Doanh Tín.
Người kiểm duyệt nội dung
PGS.TS Đặng Hoàng Phú
Cố vấn chuyên môn cấp cao tại Hóa Chất Doanh Tín. Phó Giáo sư, Giảng viên Khoa Hóa học (ĐH KHTN ĐHQG-HCM) với hơn 10 năm kinh nghiệm nghiên cứu Hóa hữu cơ & Phổ nghiệm.
Xem hồ sơ năng lực & công bố khoa học →









