Kiến thức chuyên môn
3 Cách Giải Thích Phương Trình NaCl + H₂O – Hướng Dẫn Toàn Diện 2025
Phương trình NaCl + H₂O là một trong những truy vấn cơ bản nhất trong hóa học, nhưng câu trả lời lại không hề đơn giản. Tùy thuộc vào điều kiện, nó có thể là một quá trình hòa tan vật lý hoặc một chuỗi các phản ứng hóa học phức tạp.
Bài viết này sẽ giải thích chi tiết 3 kịch bản chính của phương trình này, từ ứng dụng trong đời sống đến quy trình sản xuất công nghiệp quan trọng.
- Hòa tan trong nước: Quá trình vật lý phân ly thành ion. Phương trình: NaCl(s) ⟶ Na⁺(aq) + Cl⁻(aq).
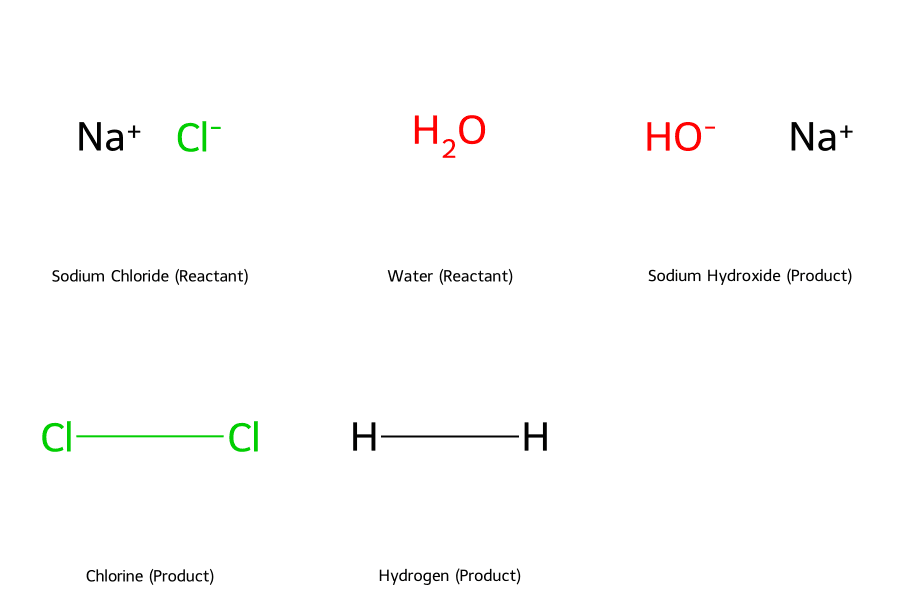
- Điện phân có màng ngăn: Sản xuất ra các hóa chất công nghiệp quan trọng. Phương trình: 2NaCl + 2H₂O ⟶ 2NaOH + Cl₂ + H₂.
- Điện phân không màng ngăn: Tạo ra nước Javel. Phương trình tổng quát: NaCl + H₂O ⟶ NaClO + H₂.
Cách 1: Hòa Tan NaCl Trong Nước (Quá trình Vật lý)
Đây là quá trình vật lý, không phải phản ứng hóa học. Muối NaCl phân ly thành các ion Na⁺ và Cl⁻ trong nước, tạo thành dung dịch muối ăn.
Đây là hiện tượng quen thuộc nhất khi bạn hòa muối ăn (NaCl) vào nước. Cần nhấn mạnh rằng đây không phải là một phản ứng hóa học mà là một quá trình hòa tan, nơi các phân tử nước bao quanh các ion Natri và Clo.
Các bước thực hiện
Chỉ cần cho muối rắn (NaCl) vào nước (H₂O) và khuấy đều. Muối sẽ tan ra, phân ly thành ion Na⁺ và Cl⁻.
Bước 1: Chuẩn bị muối Natri Clorua (NaCl) dạng rắn và nước cất (H₂O).
Bước 2: Cho NaCl vào nước và khuấy đều. Các phân tử nước, với tính chất phân cực, sẽ “kéo” các ion ra khỏi mạng tinh thể muối.
Bước 3: Quan sát sự phân ly ion. NaCl là một chất điện li mạnh, nó sẽ phân ly hoàn toàn thành các ion mang điện tích.
Trong đó: Na⁺ là cation Natri và Cl⁻ là anion Clorua.
Cách 2: Điện Phân Dung Dịch NaCl Có Màng Ngăn
Đây là một phản ứng hóa học quan trọng trong công nghiệp, sử dụng dòng điện để tạo ra Xút (NaOH), khí Clo (Cl₂) và khí Hydro (H₂). Màng ngăn dùng để tách riêng các sản phẩm, ngăn chúng phản ứng với nhau.
Đây là một quá trình hóa học thực sự, sử dụng dòng điện để phân tách các chất trong dung dịch. Phương pháp điện phân dung dịch NaCl có màng ngăn là nền tảng của ngành công nghiệp Xút-Clo, với sản lượng toàn cầu năm 2024 ước tính đạt trên 85 triệu tấn Xút.
Quy trình và phương trình phản ứng
Khi dòng điện chạy qua, nước bị khử ở cực âm (catot) tạo H₂ và OH⁻, ion Cl⁻ bị oxi hóa ở cực dương (anot) tạo khí Cl₂. Ion Na⁺ kết hợp với OH⁻ tạo thành NaOH.
Bước 1: Chuẩn bị một dung dịch NaCl bão hòa, bình điện phân có màng ngăn xốp và các điện cực trơ (ví dụ: than chì, platin).
Bước 2: Đổ dung dịch vào bình. Màng ngăn có tác dụng ngăn cách không cho các sản phẩm ở hai điện cực phản ứng với nhau.
Bước 3: Nối điện cực với nguồn điện một chiều.
- Tại Catot (cực âm): Phân tử nước nhận electron.
2H₂O + 2e⁻ ⟶ H₂ (k) + 2OH⁻ - Tại Anot (cực dương): Ion Cl⁻ nhường electron.
2Cl⁻ ⟶ Cl₂ (k) + 2e⁻
Ion Na⁺ từ dung dịch sẽ kết hợp với ion OH⁻ vừa tạo ra ở catot để hình thành Natri Hydroxit (NaOH).
2NaCl + 2H₂O ⟶ 2NaOH + Cl₂ (k) + H₂ (k)
Cách 3: Điện Phân Dung Dịch NaCl Không Có Màng Ngăn
Khi không có màng ngăn, khí Clo (Cl₂) sinh ra ở anot sẽ phản ứng ngay với dung dịch NaOH tạo thành ở catot. Phản ứng này tạo ra hỗn hợp Natri Clorua (NaCl) và Natri Hypoclorit (NaClO), chính là thành phần của nước Javel.
Khi không có màng ngăn, quá trình điện phân ban đầu vẫn diễn ra như trên, nhưng các sản phẩm sẽ tương tác với nhau ngay trong bình.
Phản ứng phụ và sản phẩm cuối cùng
Phương trình phản ứng phụ: Cl₂ + 2NaOH ⟶ NaCl + NaClO + H₂O. Sản phẩm chính của toàn bộ quá trình là nước Javel (chứa NaClO) và khí Hydro.
Bước 1 & 2: Tương tự như phương pháp trên nhưng sử dụng bình điện phân không có màng ngăn.
Bước 3: Khí Clo tạo ra ở anot sẽ ngay lập tức phản ứng với dung dịch NaOH vừa hình thành ở catot. Phản ứng này tạo ra Natri Hypoclorit (NaClO), thành phần chính của nước Javel.
NaCl + H₂O ⟶ NaClO + H₂ (k)
So Sánh 3 Cách Giải Thích
Tóm lại, hòa tan là quá trình vật lý dùng trong đời sống. Điện phân có màng ngăn là quy trình công nghiệp sản xuất hóa chất tinh khiết. Điện phân không màng ngăn dùng để sản xuất chất tẩy rửa (nước Javel).
| Tiêu Chí | Hòa Tan | Điện Phân Có Màng Ngăn | Điện Phân Không Màng Ngăn |
|---|---|---|---|
| Bản chất | Vật lý | Hóa học | Hóa học & Phản ứng phụ |
| Điều kiện | Nhiệt độ phòng | Dòng điện, màng ngăn | Dòng điện, không màng ngăn |
| Sản phẩm chính | Dung dịch NaCl (aq) | NaOH, Cl₂, H₂ | NaClO, H₂ |
| Ưu điểm | Đơn giản, nhanh | Sản phẩm tinh khiết, giá trị cao | Dễ sản xuất chất khử trùng |
| Nhược điểm | Không tạo sản phẩm mới | Cần thiết bị phức tạp | Sản phẩm không tinh khiết |
| Ứng dụng | Nấu ăn, đời sống | Sản xuất hóa chất công nghiệp | Sản xuất nước Javel |
Lưu Ý An Toàn và Sai Lầm Thường Gặp
Sai lầm phổ biến nhất là viết phương trình NaCl + H₂O → NaOH + HCl, phương trình này không xảy ra. Luôn cẩn trọng với khí Clo sinh ra khi điện phân vì đây là khí độc.
- Sai lầm kinh điển: Nhiều người cho rằng `NaCl + H₂O ⟶ NaOH + HCl`. Đây là một phương trình sai. Phản ứng này chỉ xảy ra theo chiều ngược lại (trung hòa), tức là axit HCl tác dụng với bazơ NaOH.
- Bỏ qua màng ngăn: Trong sản xuất công nghiệp, việc không có màng ngăn sẽ khiến Cl₂ phản ứng với NaOH, làm giảm hiệu suất và tạo ra sản phẩm không mong muốn.
- An toàn: Khí Clo (Cl₂) là một chất khí độc. Các thí nghiệm điện phân phải được tiến hành trong môi trường thông thoáng và có trang bị bảo hộ đầy đủ.
Câu Hỏi Thường Gặp (FAQs)
Câu 1: Tóm lại NaCl có phản ứng với H₂O không?
Trả lời: Không, nếu chỉ hòa tan thông thường. Có, khi có tác dụng của dòng điện (điện phân).
Câu 2: Điều kiện quan trọng nhất để điện phân dung dịch NaCl là gì?
Trả lời: Cần có dòng điện một chiều, điện cực trơ và dung dịch muối có nồng độ đủ cao, tốt nhất là dung dịch bão hòa.
Câu 3: Làm thế nào để cân bằng phương trình điện phân có màng ngăn?
Trả lời: Bạn có thể tham khảo hướng dẫn chi tiết về cách cân bằng phương trình NaCl + H₂O để hiểu rõ về việc bảo toàn nguyên tố và điện tích.
Câu 4: Các ứng dụng thực tế quan trọng nhất là gì?
Trả lời: Hòa tan muối ăn là ứng dụng hàng ngày. Điện phân là quy trình xương sống để sản xuất Xút và Clo, hai trong số các hóa chất được sản xuất nhiều nhất trên thế giới.
Câu 5: Có gì mới về công nghệ này trong năm 2025 không?
Trả lời: Về cơ bản, nguyên tắc hóa học không thay đổi. Tuy nhiên, các quy định mới của Luật Hóa Chất 2025 có thể sẽ tập trung vào các công nghệ điện phân tiên tiến hơn, tiết kiệm năng lượng và thân thiện với môi trường hơn.
Người kiểm duyệt nội dung
PGS.TS Đặng Hoàng Phú
Cố vấn chuyên môn cấp cao tại Hóa Chất Doanh Tín. Phó Giáo sư, Giảng viên Khoa Hóa học (ĐH KHTN ĐHQG-HCM) với hơn 10 năm kinh nghiệm nghiên cứu Hóa hữu cơ & Phổ nghiệm.
Xem hồ sơ năng lực & công bố khoa học →





