Kiến thức chuyên môn
Bảng Độ Âm Điện Hoàn Chỉnh 2025: Hướng Dẫn Chuyên Sâu Cho Ngành Hóa Chất Việt Nam
Độ âm điện là gì? Đây là một đại lượng hóa học cơ bản, đo lường khả năng của một nguyên tử trong phân tử hút electron về phía nó khi hình thành liên kết hóa học. Bảng độ âm điện theo thang Pauling, với Fluor (F) có giá trị cao nhất (3.98) và Caesium (Cs) thấp nhất (0.79), là công cụ không thể thiếu để dự đoán bản chất liên kết và tính chất của hàng ngàn hợp chất.
Tại Việt Nam, từ các nhà máy sản xuất phân đạm quy mô lớn đến các phòng thí nghiệm hóa dược và vật liệu polymer, hiểu và áp dụng chính xác thang đo này giúp tối ưu hóa quy trình và nâng cao chất lượng sản phẩm.
4 Bước Sử Dụng Bảng Độ Âm Điện Để Phân Tích Phản Ứng
Quy trình phân tích liên kết hóa học gồm 4 bước: (1) Tra cứu giá trị độ âm điện, (2) Tính hiệu số Δχ, (3) Xác định loại liên kết dựa trên khoảng giá trị của Δχ (ion, cộng hóa trị phân cực, không phân cực), và (4) Dự đoán cực tính của phân tử.
Để khai thác hiệu quả bảng giá trị này, hãy tuân thủ quy trình 4 bước đơn giản sau:
- Tra Cứu Giá Trị Độ Âm Điện: Xác định giá trị độ âm điện của các nguyên tố tham gia phản ứng từ Bảng Tuần Hoàn Hóa Học đầy đủ bên dưới.
- Tính Hiệu Độ Âm Điện (Δχ): Áp dụng công thức đơn giản: Δχ = |χA – χB|, trong đó χA và χB là độ âm điện của hai nguyên tử A và B.
- Xác Định Loại Liên Kết:
- Δχ < 0.4: Liên kết cộng hóa trị không phân cực (electron được chia sẻ đều).
- 0.4 ≤ Δχ < 1.7: Liên kết cộng hóa trị phân cực (electron lệch về phía nguyên tử có độ âm điện cao hơn).
- Δχ ≥ 1.7: Liên kết ion (electron chuyển hẳn từ nguyên tử có độ âm điện thấp sang cao).
- Dự Đoán Cực Tính Phân Tử: Nguyên tử có độ âm điện (χ) cao hơn sẽ mang điện tích âm một phần (δ−), trong khi nguyên tử còn lại mang điện tích dương một phần (δ+). Điều này quyết định đến độ tan và khả năng phản ứng của hợp chất.
Ví dụ thực tế: Xét phân tử axit clohidric (HCl). Tra bảng ta có: χCl = 3.16 và χH = 2.20.
⟶ Δχ = |3.16 – 2.20| = 0.96.
Vì 0.4 ≤ 0.96 < 1.7, đây là liên kết cộng hóa trị phân cực, với Clo (Cl) mang điện tích âm và Hydro (H) mang điện tích dương.
Ứng Dụng Chuyên Sâu Trong Ngành Hóa Chất Việt Nam
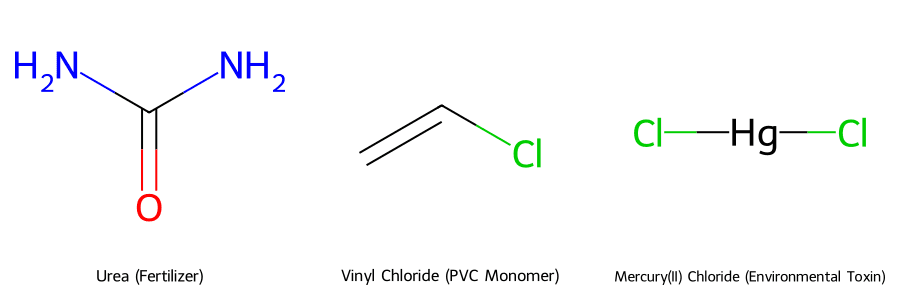
Hiệu độ âm điện được ứng dụng thực tiễn để tối ưu hóa sản xuất phân bón (Urê), nâng cao chất lượng hóa dược và vật liệu polymer (PVC), đồng thời là cơ sở khoa học để đánh giá độc tính và xử lý ô nhiễm môi trường hóa chất.
1. Sản Xuất Phân Bón
Ngành sản xuất phân bón, chiếm tới 40% giá trị ngành hóa chất Việt Nam, phụ thuộc rất nhiều vào việc tối ưu hóa các hợp chất. Ví dụ, trong phân Urê (công thức CO(NH₂)₂), hiệu độ âm điện giữa Nitơ (N) (χN=3.04) và Cacbon (C) (χC=2.55) là Δχ = 0.49. Liên kết cộng hóa trị phân cực này giúp phân tử ổn định, tránh bị ion hóa sớm và tăng hiệu quả hấp thụ dinh dưỡng cho cây trồng.
2. Hóa Dược và Polymer
Trong lĩnh vực hóa dược, Δχ giúp dự đoán hiệu quả của các liên kết. Liên kết C-F (Δχ ≈ 1.43) trong nhóm thuốc kháng sinh fluoroquinolon là một ví dụ điển hình, làm tăng hoạt tính sinh học của thuốc.
Đối với ngành công nghiệp Polymer, các nhà máy lớn như Vinachem áp dụng nguyên tắc này để thiết kế vật liệu PVC (Polyvinyl Clorua) có độ bền vượt trội nhờ liên kết C-Cl phân cực mạnh (Δχ ≈ 0.61).
3. Xử Lý Môi Trường Hóa Chất
Độ âm điện còn là một chỉ số để dự đoán độc tính. Hợp chất HgCl₂ có Δχ(Hg-Cl) = 1.07, cho thấy liên kết phân cực mạnh và dễ phân ly ra ion thủy ngân (Hg) độc hại. Dựa vào đó, các chuyên gia môi trường sử dụng các hợp chất chứa lưu huỳnh (S) (χS = 2.58) để thực hiện chelat hóa, tạo liên kết Hg-S bền vững hơn để khử độc.
Bảng Độ Âm Điện Hoàn Chỉnh Theo Thang Pauling (Cập Nhật 2025)
Dữ liệu độ âm điện theo thang Pauling được tổng hợp từ IUPAC và Allred (1961), vẫn giữ nguyên giá trị tham chiếu cốt lõi cho các nguyên tố phổ biến đến năm 2025.
| Nhóm → / Chu kỳ ↓ | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | H 2.20 | He – | ||||||||||||||||
| 2 | Li 0.98 | Be 1.57 | B 2.04 | C 2.55 | N 3.04 | O 3.44 | F 3.98 | Ne – | ||||||||||
| 3 | Na 0.93 | Mg 1.31 | Al 1.61 | Si 1.90 | P 2.19 | S 2.58 | Cl 3.16 | Ar – | ||||||||||
| 4 | K 0.82 | Ca 1.00 | Sc 1.36 | Ti 1.54 | V 1.63 | Cr 1.66 | Mn 1.55 | Fe 1.83 | Co 1.88 | Ni 1.91 | Cu 1.90 | Zn 1.65 | Ga 1.81 | Ge 2.01 | As 2.18 | Se 2.55 | Br 2.96 | Kr 3.00 |
| 5 | Rb 0.82 | Sr 0.95 | Y 1.22 | Zr 1.33 | Nb 1.60 | Mo 2.16 | Tc 1.90 | Ru 2.20 | Rh 2.28 | Pd 2.20 | Ag 1.93 | Cd 1.69 | In 1.78 | Sn 1.96 | Sb 2.05 | Te 2.10 | I 2.66 | Xe 2.60 |
| 6 | Cs 0.79 | Ba 0.89 | La-Lu* | Hf 1.30 | Ta 1.50 | W 2.36 | Re 1.90 | Os 2.20 | Ir 2.20 | Pt 2.28 | Au 2.54 | Hg 2.00 | Tl 1.62 | Pb 1.87 | Bi 2.02 | Po 2.00 | At 2.20 | Rn 2.20 |
| 7 | Fr 0.70 | Ra 0.90 | Ac-Lr** | Rf – | Db – | Sg – | Bh – | Hs – | Mt – | Ds – | Rg – | Cn – | Nh – | Fl – | Mc – | Lv – | Ts – | Og – |
* Lanthanides (La-Lu): La 1.10, Ce 1.12, Pr 1.13, Nd 1.14, Pm 1.13, Sm 1.17, Eu 1.20, Gd 1.20, Tb 1.10, Dy 1.22, Ho 1.23, Er 1.24, Tm 1.25, Yb 1.10, Lu 1.27.
** Actinides (Ac-Lr): Ac 1.10, Th 1.30, Pa 1.50, U 1.38, Np 1.36, Pu 1.28, Am 1.13, Cm 1.28, Bk 1.30, Cf 1.30, Es 1.30, Fm 1.30, Md 1.30, No 1.30, Lr 1.30.
Những Lưu Ý Quan Trọng Khi Sử Dụng Bảng
Khi sử dụng bảng độ âm điện, cần lưu ý đến trạng thái lai hóa của nguyên tử vì nó ảnh hưởng đến giá trị độ âm điện. Đồng thời, nhận biết các cặp nguyên tố có hiệu độ âm điện lớn để đảm bảo an toàn trong phòng thí nghiệm và tận dụng công nghệ để tính toán chính xác.
- Sai lầm về lai hóa (Hybridization): Độ âm điện của một nguyên tố không phải là hằng số tuyệt đối. Nó thay đổi tùy thuộc vào trạng thái lai hóa. Ví dụ, Cacbon trong CH₄ (lai hóa sp³) có χ ≈ 2.48, nhưng trong CO₂ (lai hóa sp) thì χ ≈ 2.75. Luôn kiểm tra cấu trúc phân tử để có dự đoán chính xác nhất.
- An toàn trong phòng thí nghiệm: Những phản ứng giữa các nguyên tố có Δχ rất lớn (ví dụ: Na và Cl₂, Δχ ≈ 2.23) thường là phản ứng tỏa nhiệt và rất mãnh liệt. Việc hiểu rõ điều này giúp tuân thủ các quy định an toàn về hóa chất, đặc biệt khi làm việc với các kim loại kiềm và halogen.
- Tích hợp công nghệ: Các phần mềm chuyên dụng như ChemDraw có thể tự động tính toán Δχ và mô phỏng cực tính phân tử, giúp giảm thiểu sai sót trong quá trình nghiên cứu và thiết kế hợp chất.
Câu Hỏi Thường Gặp (FAQs)
Độ âm điện dùng để làm gì?
Nó là đại lượng cốt lõi để dự đoán một liên kết sẽ là ion, cộng hóa trị phân cực hay không phân cực, từ đó suy ra các tính chất quan trọng như độ tan, nhiệt độ nóng chảy, và khả năng phản ứng hóa học.
Làm thế nào để áp dụng trong ngành hóa chất tại Việt Nam?
Kiến thức về độ âm điện giúp tối ưu hóa công thức phân bón Urê, thiết kế vật liệu polymer PVC bền hơn, và phát triển các loại dung môi phù hợp cho từng ứng dụng cụ thể.
Giá trị trong bảng có thay đổi vào năm 2025 không?
Không có thay đổi lớn nào được dự kiến cho các nguyên tố phổ biến. Thang đo Pauling đã rất ổn định. Tuy nhiên, các nhà khoa học vẫn đang tiếp tục nghiên cứu và tinh chỉnh giá trị cho các nguyên tố siêu nặng (từ Rf trở đi).
Sai lầm phổ biến nhất khi dùng độ âm điện là gì?
Sai lầm lớn nhất là bỏ qua trạng thái lai hóa của nguyên tử, dẫn đến dự đoán sai về cực tính của liên kết. Luôn xem xét cấu trúc không gian của phân tử để có kết quả chính xác.
Nếu bạn cần tư vấn sâu hơn hoặc tìm mua các loại hóa chất công nghiệp và thí nghiệm, hãy truy cập website của chúng tôi để được hỗ trợ.
Người kiểm duyệt nội dung
PGS.TS Đặng Hoàng Phú
Cố vấn chuyên môn cấp cao tại Hóa Chất Doanh Tín. Phó Giáo sư, Giảng viên Khoa Hóa học (ĐH KHTN ĐHQG-HCM) với hơn 10 năm kinh nghiệm nghiên cứu Hóa hữu cơ & Phổ nghiệm.
Xem hồ sơ năng lực & công bố khoa học →









