Kiến thức chuyên môn
Ankadien Là Gì? Tính Chất, Điều Chế & Ứng Dụng Công Nghiệp
Để hiểu rõ ankadien là gì, bạn có thể nắm bắt ngay định nghĩa cốt lõi: Ankadien là những hidrocacbon không no, mạch hở, có công thức chung là CnH2n-2 (với n ≥ 3), trong phân tử chứa hai liên kết đôi C=C. Dựa vào vị trí của hai liên kết đôi này, ankadien được chia thành 3 loại với các tính chất đặc trưng khác nhau.
Bài viết này sẽ cung cấp toàn bộ kiến thức hóa học cần thiết về ankadien, từ công thức, cách gọi tên, phân loại đến các tính chất hóa học và ứng dụng quan trọng trong công nghiệp.
Công Thức Chung và Đồng Phân Của Ankadien là gì?
Ankadien có công thức chung là CnH2n-2 (n ≥ 3) và có hai loại đồng phân chính là đồng phân cấu tạo (vị trí liên kết đôi, mạch carbon) và đồng phân hình học (cis-trans).
1. Công thức phân tử chung của Ankadien được xác định như thế nào?
Công thức chung của ankadien là CnH2n-2 với điều kiện n ≥ 3. Điều này có nghĩa là phân tử ankadien đầu tiên trong dãy đồng đẳng phải có ít nhất 3 nguyên tử carbon.
- C₃H₄ (Propadien, Allen)
- C₄H₆ (Butadien)
- C₅H₈ (Pentadien, Isopren)
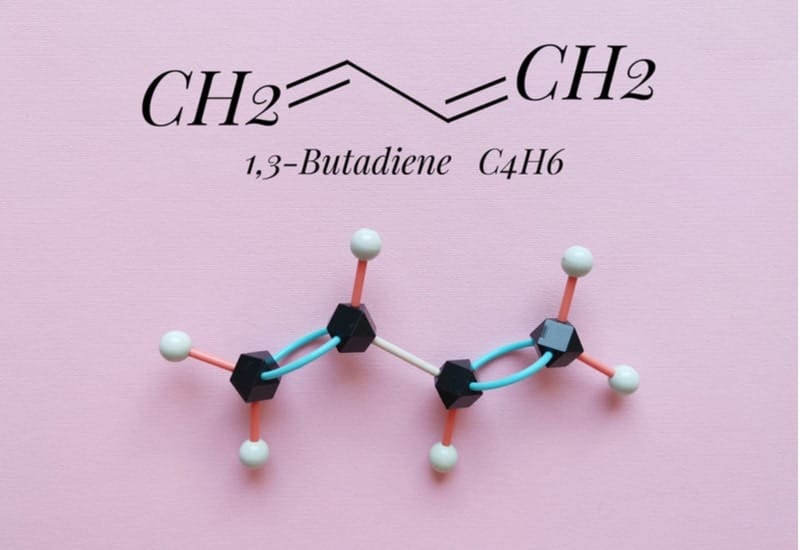
2. Ankadien có những loại đồng phân nào?
Ankadien có hai loại đồng phân chính, tạo nên sự đa dạng trong cấu trúc của chúng:
- Đồng phân cấu tạo: Bao gồm đồng phân về vị trí liên kết đôi và đồng phân về mạch carbon. Các liên kết trong phân tử này đều là liên kết cộng hóa trị.
- Đồng phân hình học (cis-trans): Xảy ra khi mỗi nguyên tử carbon ở liên kết đôi liên kết với hai nhóm thế khác nhau.
Ví dụ: Các đồng phân của C₄H₆ bao gồm Buta-1,3-dien và Buta-1,2-dien.
Cách Gọi Tên Ankadien Theo Danh Pháp IUPAC như thế nào?
Tên ankadien theo IUPAC được gọi bằng cách chọn mạch carbon dài nhất chứa cả hai liên kết đôi, đánh số ưu tiên liên kết đôi, và gọi tên theo cấu trúc: (Vị trí nhánh)-(Tên nhánh) + (Tên ankan mạch chính) + a + -(vị trí liên kết đôi)-dien.
Việc gọi tên ankadien theo danh pháp IUPAC tuân theo một quy trình rõ ràng để đảm bảo tính nhất quán và chính xác trên toàn cầu.
Các bước gọi tên:
- Chọn mạch chính: Là mạch carbon dài nhất chứa cả hai liên kết đôi.
- Đánh số thứ tự: Bắt đầu đánh số từ phía gần liên kết đôi hơn để tổng số chỉ vị trí liên kết đôi là nhỏ nhất.
- Gọi tên:
(Số chỉ vị trí nhánh)-(Tên nhánh) + (Tên ankan tương ứng với mạch chính) + a + -(số chỉ vị trí liên kết đôi)-dien
Lưu ý: Thêm chữ “a” vào sau tên ankan mạch chính để dễ đọc (ví dụ: Butan -> Buta). So với Ankan, cách gọi tên ankadien phức tạp hơn do sự hiện diện của nhiều liên kết đôi.
Ví dụ:
- CH₂=CH-CH=CH₂: Buta-1,3-dien
- CH₂=C(CH₃)-CH=CH₂: 2-metylbuta-1,3-dien (thường gọi là Isopren)
Ankadien được Phân Loại như thế nào?
Ankadien được phân thành ba loại chính dựa vào vị trí tương đối của hai liên kết đôi: ankadien liên hợp (cách nhau một liên kết đơn), ankadien không liên hợp (cách nhau nhiều hơn một liên kết đơn), và ankadien liền kề (nằm cạnh nhau).
Đây là phần kiến thức cực kỳ quan trọng vì nó quyết định tính chất hóa học đặc trưng và các ứng dụng khác nhau của từng loại ankadien.
| Loại Ankadien | Cấu Trúc | Đặc Điểm | Ví dụ |
|---|---|---|---|
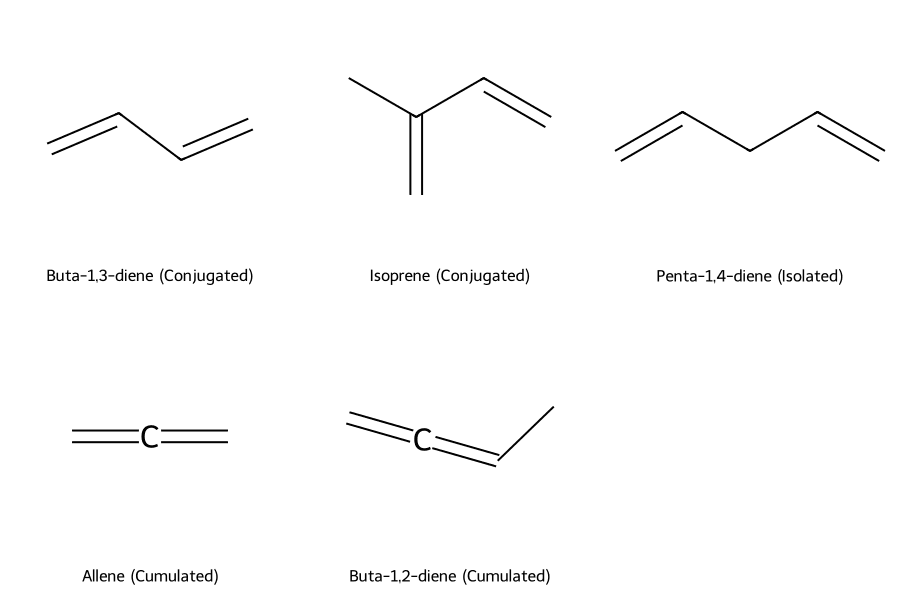
| Ankadien liên hợp | C=C-C=C | Hai liên kết đôi cách nhau bởi một liên kết đơn. Hệ liên hợp này rất bền vững do hiệu ứng cộng hưởng electron. | Buta-1,3-dien, Isopren |
| Ankadien không liên hợp | C=C-(C)n-C=C | Hai liên kết đôi cách nhau bởi hai hay nhiều liên kết đơn. Các liên kết đôi hoạt động độc lập như anken. | Penta-1,4-dien |
| Ankadien liền kề | C=C=C | Hai liên kết đôi nằm cạnh nhau. Carbon ở giữa có lai hóa sp, hai carbon còn lại có lai hóa sp². | Propadien (Allen) |
Tính Chất Hóa Học Đặc Trưng Của Ankadien là gì?
Ankadien có các tính chất hóa học đặc trưng bao gồm phản ứng cộng (với H₂, Br₂, HX), phản ứng trùng hợp tạo polime (đặc biệt là cao su tổng hợp), và phản ứng oxy hóa (cháy hoàn toàn hoặc làm mất màu dung dịch KMnO₄).
Ankadien tham gia vào các phản ứng hóa học tương tự anken như phản ứng cộng, trùng hợp và oxy hóa. Tuy nhiên, sự khác biệt lớn nằm ở ankadien liên hợp, nơi hiệu ứng liên hợp tạo ra các sản phẩm độc đáo.
1. Phản ứng cộng (H₂, Br₂, HX) diễn ra như thế nào?
Đây là phản ứng quan trọng nhất. Khi cộng với các tác nhân như Brom (Br₂) hay HX, ankadien liên hợp cho ra sản phẩm theo những cách đặc biệt.
Đối với ankadien liên hợp (ví dụ: Buta-1,3-dien):
Phản ứng có thể xảy ra theo hai hướng song song do hiệu ứng liên hợp:
- Cộng 1,2: Tác nhân cộng vào 2 carbon liền kề của một liên kết đôi.
- Cộng 1,4: Tác nhân cộng vào 2 carbon ở hai đầu của hệ liên hợp.
Ảnh hưởng của nhiệt độ đến sản phẩm:
- Ở nhiệt độ thấp (-80°C): Ưu tiên tạo ra sản phẩm cộng 1,2 (sản phẩm động học, tạo thành nhanh hơn).
CH₂=CH−CH=CH₂ + HBr ⟶ CH₃−CH(Br)−CH=CH₂ (Sản phẩm chính) - Ở nhiệt độ cao (40°C): Ưu tiên tạo ra sản phẩm cộng 1,4 (sản phẩm nhiệt động học, bền vững hơn).
CH₂=CH−CH=CH₂ + HBr ⟶ CH₃−CH=CH−CH₂Br (Sản phẩm chính)
2. Phản ứng trùng hợp của Ankadien có ý nghĩa gì?
Đây là tính chất tạo nên giá trị kinh tế lớn nhất của ankadien. Dưới tác dụng của nhiệt độ, áp suất và chất xúc tác, ankadien liên hợp tham gia phản ứng trùng hợp để tạo thành các polymer có khối lượng phân tử lớn.
Ví dụ: Trùng hợp buta-1,3-dien tạo ra polibutadien (cao su Buna).
nCH₂=CH−CH=CH₂ ⟶ (−CH₂−CH=CH−CH₂−)n
3. Phản ứng oxy hóa của Ankadien xảy ra ra sao?
- Oxy hóa hoàn toàn (Phản ứng cháy): Ankadien cháy trong oxy tạo ra CO₂ và H₂O.
CnH2n-2 + (3n-1)/2 O₂ ⟶ nCO₂ + (n-1)H₂O - Oxy hóa không hoàn toàn: Tương tự anken, ankadien làm mất màu dung dịch KMnO₄, đây là phản ứng dùng để nhận biết chúng.
So Sánh Ankadien, Anken và Ankin có gì khác biệt?
Sự khác biệt chính nằm ở số lượng và loại liên kết không no: Anken có một liên kết đôi, Ankadien có hai liên kết đôi, và Ankin có một liên kết ba. Điều này dẫn đến sự khác nhau trong công thức chung và tính chất hóa học đặc trưng của chúng.
Để hệ thống hóa kiến thức, bảng so sánh sau sẽ giúp bạn phân biệt rõ ràng các hidrocacbon không no phổ biến.
| Tiêu Chí | Anken | Ankadien | Ankin |
|---|---|---|---|
| Công thức chung | CnH2n (n ≥ 2) | CnH2n-2 (n ≥ 3) | CnH2n-2 (n ≥ 2) |
| Đặc điểm cấu tạo | Một liên kết đôi C=C | Hai liên kết đôi C=C | Một liên kết ba C≡C |
| Phản ứng đặc trưng | Phản ứng cộng | Phản ứng cộng (1,2 và 1,4), trùng hợp | Phản ứng cộng, phản ứng thế với ion kim loại (ank-1-in) |
Ankadien được Điều Chế và có Ứng Dụng Quan Trọng nào?
Ankadien được điều chế chủ yếu bằng phương pháp dehydro hóa ankan tương ứng. Ứng dụng quan trọng nhất của chúng là làm monome để sản xuất các loại cao su tổng hợp như cao su Buna và poliisopren.
1. Ankadien được điều chế bằng phương pháp nào?
Trong công nghiệp, ankadien được điều chế chủ yếu bằng phương pháp dehydro hóa (tách hydro) từ các ankan tương ứng có sẵn trong dầu mỏ và khí thiên nhiên.
Ví dụ: Điều chế buta-1,3-dien và isopren từ butan và isopentan.
- CH₃−CH₂−CH₂−CH₃ ⟶ CH₂=CH−CH=CH₂ + 2H₂
- CH₃−CH(CH₃)−CH₂−CH₃ ⟶ CH₂=C(CH₃)−CH=CH₂ + 2H₂
2. Các ứng dụng chính của Ankadien là gì?
Ứng dụng lớn nhất và quan trọng nhất của ankadien là làm monome để sản xuất polime, đặc biệt là các loại cao su tổng hợp, một vật liệu không thể thiếu trong đời sống hiện đại và sản xuất công nghiệp:
- Buta-1,3-dien: Dùng để sản xuất cao su Buna, cao su Buna-S (đồng trùng hợp với stiren), cao su Buna-N (đồng trùng hợp với acrylonitrin). Các loại cao su này được dùng làm lốp xe, ống dẫn, gioăng, và nhiều sản phẩm khác.
- Isopren (2-metylbuta-1,3-dien): Trùng hợp tạo ra poliisopren, có cấu trúc tương tự cao su thiên nhiên, được sử dụng trong các ứng dụng đòi hỏi tính đàn hồi cao.
Các Câu Hỏi Thường Gặp (FAQ) về Ankadien
1. Ankadien liên hợp có gì đặc biệt?
Ankadien liên hợp đặc biệt bền vững và có khả năng phản ứng cộng ở vị trí 1,4 do có hệ liên kết π liên hợp trên toàn bộ khung C=C-C=C.
Hệ liên hợp này cho phép các electron π giải tỏa trên bốn nguyên tử carbon, làm cho phân tử bền hơn và tạo ra một cơ chế phản ứng độc đáo không thấy ở các hidrocacbon không no khác.
2. Tại sao phản ứng cộng vào ankadien liên hợp lại phụ thuộc vào nhiệt độ?
Sự phụ thuộc vào nhiệt độ là do sự cạnh tranh giữa sản phẩm động học (tạo thành nhanh hơn, ưu tiên ở nhiệt độ thấp) và sản phẩm nhiệt động học (bền vững hơn, ưu tiên ở nhiệt độ cao).
Phản ứng tạo ra hai sản phẩm (cộng 1,2 và cộng 1,4) với tốc độ và độ bền khác nhau. Ở nhiệt độ thấp, phản ứng ưu tiên sản phẩm tạo thành nhanh hơn (yếu tố động học). Ở nhiệt độ cao, hệ thống có đủ năng lượng để ưu tiên tạo thành sản phẩm bền vững hơn (yếu tố nhiệt động học).
3. Ankadien quan trọng nhất trong công nghiệp là gì?
Buta-1,3-dien và Isopren là hai ankadien quan trọng nhất về mặt thương mại.
Chúng là những khối xây dựng cơ bản cho ngành công nghiệp sản xuất cao su tổng hợp trên toàn thế giới, với sản lượng hàng triệu tấn mỗi năm, phục vụ cho ngành công nghiệp ô tô, hàng tiêu dùng và nhiều lĩnh vực khác.
Người kiểm duyệt nội dung
PGS.TS Đặng Hoàng Phú
Cố vấn chuyên môn cấp cao tại Hóa Chất Doanh Tín. Phó Giáo sư, Giảng viên Khoa Hóa học (ĐH KHTN ĐHQG-HCM) với hơn 10 năm kinh nghiệm nghiên cứu Hóa hữu cơ & Phổ nghiệm.
Xem hồ sơ năng lực & công bố khoa học →









