Kiến thức chuyên môn
Dung dịch là gì? Khái niệm, đặc điểm và ứng dụng trong đời sống
Dung dịch là một hỗn hợp đồng nhất giữa chất tan và dung môi, thường ở trạng thái lỏng, với chất tan phân bố đều trong dung môi (ví dụ: nước muối, nước đường). Bài viết này cung cấp hướng dẫn chi tiết về phân loại, đặc điểm, tính chất, ứng dụng và các yếu tố ảnh hưởng đến dung dịch, kèm phương pháp pha chế cụ thể.
Định Nghĩa Dung Dịch
Dung dịch là một hỗn hợp đồng nhất, trong đó chất tan (như muối, đường) hòa tan hoàn toàn vào dung môi (như nước) để tạo thành một pha duy nhất, không thể phân biệt bằng mắt thường.

Dung dịch là một hỗn hợp đồng nhất, trong đó chất tan (substance to be dissolved) hòa lẫn hoàn toàn trong dung môi (solvent) tạo thành một pha duy nhất. Khác với huyền phù, các hạt chất tan trong dung dịch phân bố ở mức độ phân tử hoặc ion và không thể nhìn thấy bằng mắt thường.
Ví dụ kinh điển nhất là muối NaCl (Natri Clorua) hòa tan trong nước tạo thành dung dịch nước muối. Dung dịch có thể tồn tại ở nhiều trạng thái:
- Lỏng: Nước đường, cồn y tế.
- Rắn: Các loại hợp kim như gang, thép.
- Khí: Không khí (Oxy, Nito…), hoặc khí CO2 hòa tan trong nước ngọt.
Phân Loại Dung Dịch
Dung dịch được phân loại chính theo độ bão hòa (chưa bão hòa, bão hòa, quá bão hòa) và khả năng dẫn điện (dung dịch điện ly chứa ion và dung dịch không điện ly không chứa ion).
Dung dịch được phân loại dựa trên nhiều tiêu chí, nhưng phổ biến nhất là dựa vào độ bão hòa và khả năng dẫn điện.
Phân loại theo độ bão hòa
Phân loại theo độ bão hòa gồm 3 loại: chưa bão hòa (còn thể hòa tan thêm), bão hòa (đã hòa tan tối đa), và quá bão hòa (hòa tan vượt mức tối đa, không bền).
- Dung dịch chưa bão hòa: Là dung dịch vẫn còn khả năng hòa tan thêm chất tan ở điều kiện nhiệt độ và áp suất nhất định.
- Dung dịch bão hòa: Chứa lượng chất tan tối đa có thể hòa tan ở điều kiện cụ thể. Khi đạt đến trạng thái bão hòa, dung dịch không thể hòa tan thêm chất tan.
- Dung dịch quá bão hòa: Chứa lượng chất tan vượt quá mức bão hòa. Đây là trạng thái không bền, chất tan dư thừa rất dễ bị kết tinh (kết tủa) khi có tác động nhẹ.
Phân loại theo tính chất chất tan
Phân loại theo tính chất gồm 2 loại: dung dịch điện ly (chứa ion, dẫn điện, gồm axit, bazo, muối) và dung dịch không điện ly (không chứa ion, không dẫn điện, như dung dịch đường).
- Dung dịch điện ly: Chứa các ion tự do, có khả năng dẫn điện. Các chất điện ly thường là axit, bazo và muối. Ví dụ: Dung dịch axit sunfuric (H2SO4), dung dịch NaOH. Quá trình hòa tan NaCl trong nước (NaCl + H2O) tạo ra ion Na+ và Cl-, làm dung dịch có tính dẫn điện.
- Dung dịch không điện ly: Không chứa ion tự do, không dẫn điện. Ví dụ: Dung dịch đường Glucose hoặc Sucrose.
Thành Phần của Dung Dịch
Mọi dung dịch đều có hai thành phần chính: Chất tan (chất bị hòa tan, ví dụ: muối, đường) và Dung môi (chất dùng để hòa tan, ví dụ: nước, cồn).
Mọi dung dịch đều được cấu tạo từ hai thành phần cơ bản:
- Chất tan: Là thành phần được hòa tan, có thể là chất rắn (như đường, muối), chất lỏng (như Ethanol), hoặc chất khí (như Amoniac (NH3)).
- Dung môi: Là chất có vai trò hòa tan chất tan. Nước là dung môi phân cực phổ biến nhất. Ngoài ra, còn có nhiều dung môi công nghiệp không phân cực khác như Toluene, Xylene, và Methanol.
Đặc Điểm của Dung Dịch
Câu trả lời ngắn: Đặc điểm cơ bản của dung dịch là tính đồng nhất (thành phần giống nhau ở mọi vị trí), tính trong suốt (có thể có màu nhưng cho ánh sáng đi qua), và không thể tách chất tan bằng phương pháp lọc cơ học.
Dung dịch có những đặc điểm nhận biết cơ bản sau:
- Tính đồng nhất: Thành phần được phân bố đều trong toàn bộ dung dịch. Bất kỳ phần nào của dung dịch cũng có thành phần và tính chất như nhau.
- Tính trong suốt: Thường trong suốt, cho phép ánh sáng đi qua. Tuy nhiên, dung dịch có thể có màu tùy thuộc vào chất tan (ví dụ: dung dịch thuốc tím (KMnO4) có màu tím đặc trưng).
- Không thể tách rời bằng phương pháp cơ học: Không thể lọc chất tan ra khỏi dung môi bằng giấy lọc thông thường.
- Khả năng thay đổi nồng độ: Có thể điều chỉnh độ “đậm đặc” bằng cách thêm chất tan hoặc thêm dung môi.
Tính Chất Vật Lý của Dung Dịch
Câu trả lời ngắn: Khi tạo dung dịch, tính chất vật lý của dung môi bị thay đổi: nhiệt độ sôi tăng, nhiệt độ đông đặc giảm, áp suất hơi giảm và tỷ trọng (khối lượng riêng) thường tăng lên. Dung dịch điện ly có thêm tính chất dẫn điện.
Sự hiện diện của chất tan làm thay đổi nhiều tính chất vật lý của dung môi nguyên chất:
- Độ dẫn điện: Chỉ các dung dịch điện ly (chứa ion của axit, bazo, muối như HCl) mới có khả năng dẫn điện.
- Nhiệt độ sôi/đông đặc: So với dung môi nguyên chất, dung dịch có nhiệt độ sôi cao hơn và nhiệt độ đông đặc thấp hơn. (Ví dụ: Nước muối sôi ở >100°C và đông đặc ở <0°C).
- Áp suất hơi: Giảm đi, do các phân tử chất tan chiếm không gian trên bề mặt, cản trở sự bay hơi của dung môi.
- Khối lượng riêng: Thường tăng khi nồng độ chất tan tăng. Khái niệm này liên quan chặt chẽ đến tỷ trọng.
Tính Chất Hóa Học của Dung Dịch
Về mặt hóa học, dung dịch là hỗn hợp ổn định. Tính chất hóa học của nó là tổng hợp tính chất của dung môi và chất tan. Dung dịch điện ly cho phép các ion (cation, anion) di chuyển tự do, tạo môi trường cho các phản ứng hóa học xảy ra.
- Tính ổn định: Dung dịch là hỗn hợp ổn định về mặt hóa học.
- Phương pháp tách: Chỉ có thể tách chất tan và dung môi bằng các phương pháp vật lý như bay hơi, cô cạn hoặc chưng cất.
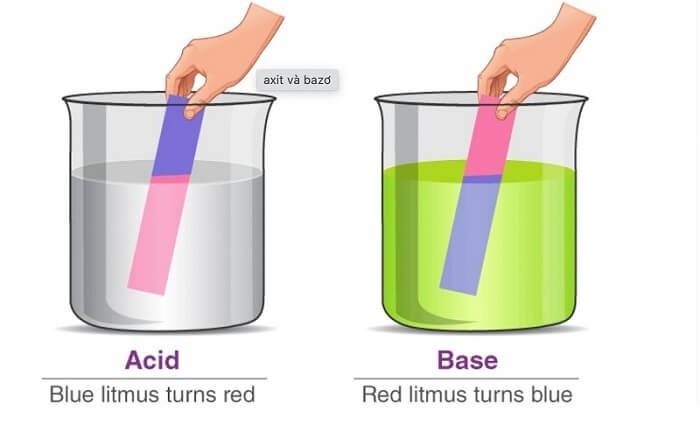
- Khả năng ion hóa: Trong dung dịch điện ly, các ion (như cation) có thể di chuyển tự do, cho phép các phản ứng hóa học xảy ra (ví dụ: phản ứng trung hòa).
- Phản ứng: Tính chất hóa học của dung dịch là tập hợp tính chất của dung môi và chất tan. Ví dụ: dung dịch NaOH (Xút lỏng) thể hiện đầy đủ tính chất của một bazo mạnh.
Ứng Dụng của Dung Dịch
Dung dịch có ứng dụng vô vàn: từ sản xuất thực phẩm (nước mắm, siro), y tế (truyền dịch, thuốc), công nghiệp (sản xuất H2SO4, NaOH), đến các quy trình thí nghiệm và xử lý nước.
Dung dịch có mặt trong mọi khía cạnh của đời sống và sản xuất:
- Sản xuất thực phẩm: Dung dịch đường, muối dùng để tạo vị, bảo quản. Các dung dịch axit hữu cơ như Acid Citric được dùng làm chất điều vị.
- Nước giải khát: Dung dịch CO2 trong nước (tạo ga). Dung dịch H3PO4 85% được dùng để tạo vị chua trong nhiều loại nước ngọt.
- Y tế và dược phẩm: Dung dịch nước muối sinh lý (NaCl 0.9%) dùng để truyền dịch. Các dung dịch khử khuẩn như Chloramin B hay Javen được pha chế ở nồng độ thích hợp.
- Hóa chất công nghiệp: Dung dịch H2SO4 dùng sản xuất phân bón, ắc quy. Dung dịch NaOH dùng trong xử lý nước, sản xuất giấy.
- Nghiên cứu và thí nghiệm: Dung dịch đệm (buffer) để duy trì pH ổn định. Các dung dịch chất chỉ thị như Phenolphthalein được dùng để xác định điểm cuối trong chuẩn độ.
Yếu Tố Ảnh Hưởng Đến Độ Tan
Các yếu tố chính ảnh hưởng đến độ tan là: bản chất của chất tan và dung môi (giống hòa tan giống), nhiệt độ (tăng nhiệt độ thường tăng độ tan chất rắn, giảm độ tan chất khí), và áp suất (chỉ ảnh hưởng lớn đến độ tan chất khí).
Độ tan là gì? Các yếu tố ảnh hưởng
Độ tan là lượng chất tan tối đa có thể hòa tan trong dung môi ở điều kiện nhất định để tạo thành dung dịch bão hòa. Nó bị ảnh hưởng bởi bản chất chất tan/dung môi, nhiệt độ, và áp suất.
Độ tan là lượng chất tan tối đa có thể hòa tan trong một lượng dung môi nhất định để tạo thành dung dịch bão hòa ở điều kiện cụ thể. Các yếu tố chính ảnh hưởng đến độ tan bao gồm:
1. Bản chất của chất tan và dung môi:
Nguyên tắc “Like dissolves like” (Giống hòa tan giống): Chất phân cực (như muối ăn NaCl) tan tốt trong dung môi phân cực (nước). Chất không phân cực (như dầu mỡ) tan tốt trong dung môi không phân cực (như Toluene hoặc White Spirit).
2. Nhiệt độ:
Chất rắn: Đa số chất rắn có độ tan tăng khi nhiệt độ tăng (ví dụ: đường Sucrose tan trong nước nóng nhanh và nhiều hơn nước lạnh).
Chất khí: Độ tan của chất khí (như CO2) giảm khi nhiệt độ tăng (Nước ngọt để nóng sẽ bị “nhạt” và mất ga).
3. Áp suất:
Chất khí: Độ tan của chất khí tăng khi áp suất của khí đó lên bề mặt chất lỏng tăng (Định luật Henry). Đây là lý do nước ngọt được nén CO2 ở áp suất cao.
Chất rắn/lỏng: Áp suất hầu như không ảnh hưởng đến độ tan.
4. Sự khuấy trộn: Khuấy trộn làm tăng tốc độ hòa tan (giúp chất tan tiếp xúc với dung môi nhanh hơn) nhưng không làm thay đổi độ tan bão hòa.
Nồng Độ Dung Dịch
Nồng độ dung dịch là đại lượng cho biết lượng chất tan có trong một lượng dung dịch xác định. Hai loại phổ biến nhất là Nồng độ phần trăm (C%) và Nồng độ mol (CM).
Nồng độ biểu thị lượng chất tan có trong một đơn vị dung dịch, quyết định độ “đậm đặc” hay “loãng” của dung dịch.
- Nồng độ phần trăm (C%):
- Công thức: C% = (Khối lượng chất tan / Khối lượng dung dịch) × 100%
- Ví dụ: Dung dịch NaCl 5% nghĩa là có 5g NaCl trong 100g dung dịch (bao gồm 5g NaCl và 95g nước).
- Nồng độ mol (CM):
- Công thức: CM = Số mol chất tan / Thể tích dung dịch (lít)
- Ví dụ: Dung dịch HCl 1M nghĩa là có 1 mol HCl trong 1 lít dung dịch.
Phương Pháp Pha Chế Dung Dịch
Có hai cách pha chế chính: theo nồng độ C% (cân khối lượng chất tan và dung môi) và theo nồng độ mol CM (cân chất tan rồi thêm dung môi vào bình định mức cho đủ thể tích). Ngoài ra còn có phương pháp pha loãng từ dung dịch đặc hơn (dùng công thức C1V1 = C2V2).
Pha chế dung dịch là một kỹ năng cơ bản trong hóa học và công nghiệp, đòi hỏi sự chính xác.
1. Pha chế theo nồng độ phần trăm:
- Bước 1: Tính toán khối lượng chất tan và khối lượng dung môi dựa trên công thức C%.
- Bước 2: Cân chính xác chất tan, sau đó cân dung môi.
- Bước 3: Hòa tan và khuấy đều.
2. Pha chế theo nồng độ mol:
- Bước 1: Tính số mol chất tan cần dùng (n = CM × V).
- Bước 2: Tính khối lượng chất tan (m = n × M).
- Bước 3: Cân chất tan, cho vào bình định mức. Thêm một ít dung môi, lắc cho tan. Thêm dung môi từ từ cho đến khi đạt vạch thể tích chính xác. Cần sử dụng các dụng cụ đo lường chính xác như pipette.
3. Pha loãng hoặc cô đặc:
- Pha loãng: Thêm dung môi (nước) để giảm nồng độ. Áp dụng quy tắc: C1V1 = C2V2.
- Cô đặc: Loại bỏ dung môi (bằng cách cô cạn hoặc đun nóng) hoặc thêm chất tan.
4. Pha chế dung dịch đặc biệt:
- Dung dịch thủy canh: Yêu cầu pha chế nhiều loại muối dinh dưỡng (như Calcium Nitrate (Ca(NO3)2) hoặc Potassium Nitrate (KNO3)) theo tỷ lệ chính xác.
Kết Luận
Dung dịch là nền tảng của vô số quá trình hóa học và sinh học. Từ dung dịch nước muối trong y tế, xút lỏng (NaOH) trong công nghiệp, đến các hóa chất xử lý nước, dung dịch hiện diện ở khắp mọi nơi. Hiểu rõ định nghĩa, phân loại, tính chất và cách pha chế dung dịch là chìa khóa để ứng dụng chúng một cách an toàn và hiệu quả.
Để tìm hiểu thêm về các loại hóa chất công nghiệp và dung môi chuyên dụng, hãy truy cập website của Hóa chất Doanh Tín hoặc liên hệ trực tiếp để được tư vấn kỹ thuật.





